Функция внешнего дыхания, газообмен и легочная гемодинамика у больных с синдромом обструктивного апноэ во сне
Первоначально синдром обструктивного апноэ во сне (СОАС) стал широко известен именно своими сердечно-легочными осложнениями. В клинической картине, описанной
C. S. Burwell et al. (1956) под названием “синдром Пиквика”, доминировали признаки правосердечной недостаточности, гиповентиляции, полицитемии и дневной сонливости на фоне ожирения (15). Однако в настоящее время ясно, что подобная клиническая картина может возникнуть в результате нескольких различных патологических состояний. В первую очередь это собственно СОАС, который часто сочетается с избыточным весом и синдром альвеолярной гиповентиляции у больных с ожирением. Таким образом, на сегодняшний день термин «синдром Пиквика» представляет преимущественно исторический интерес. Его, вероятно, следует исключить из употребления или, по крайней мере, детализировать в каждом конкретном случае. При наличии обструктивных апноэ логично было бы говорить об альвеолярной гиповентиляции у больного с СОАС и ожирением, особенно учитывая тот факт, что избыточный вес и повторные апноэ сами могут являться причиной хронической дыхательной недостаточности.
Хотя СОАС отнюдь не всегда представлен классическим симптомокомплексом, который наблюдали C. S. Burwell с соавторами, тем не менее, наличие обструктивных нарушений дыхания во время сна достаточно часто становится причиной различных кардиореспираторных расстройств, многие из которых могут приводить к ранней инвалидизации и даже преждевременной смерти этих больных.
Выявляемые у пациентов с СОАС нарушения вентиляционной функции легких большей частью достаточно неспецифичны и не имеют отношения к имеющимся у них нарушениям дыхания во время сна. Характер изменений функции внешнего дыхания у них в первую очередь определяется степенью ожирения и сопутствующей бронхолегочной
патологией (7).
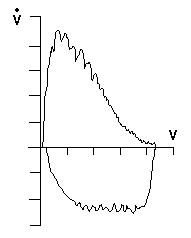 Рис. 1. Кривая “поток‑объем” у пациента с СОАС – симптом | Существует ряд признаков, которые отражают имеющиеся у больных с СОАС аномалии верхних дыхательных путей и могут косвенно свидетельствовать о возможном наличии обструктивных нарушений дыхания во время сна. Это увеличение показателя отношения максимального экспираторного потока к максимальному инспираторному потоку на уровне 50% форсированной жизненной емкости легких (MEF50%/MIF50%) больше 1, являющегося признаком сужения верхних дыхательных путей (28), и наличие низкоамплитудной зазубренности на кривой форсированного вдоха и/или выдоха, получившее в англоязычной литературе название симптома “зубьев пилы” (рис.1), появление которой отражает колебания тканей верхних дыхательных путей и свидетельствует о некоторой их нестабильности при дыхании (48). |
Однако на практике эти изменения наблюдаются лишь у части больных и не являются характерными только для СОАС (7; 32; 58), что существенно снижает их диагностическую ценность.
Результаты исследования функции внешнего дыхания не позволяют предсказывать присутствие СОАС и, следовательно, не могут служить скрининговым методом при диагностике обструктивных нарушений дыхания во время сна (16; 31).
Сопровождающая апноэ гипоксемия (рис.2) является типичным признаком этого состояния, синхронизирована с эпизодами апноэ и вследствие этого носит циклический характер (43).
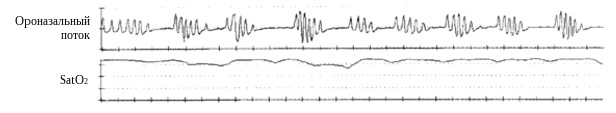
Рис. 2. Ассоциированные с респираторными паузами эпизоды десатурации у пациента с СОАС.
Эти изменения настолько характерны, что во многих случаях позволяют диагностировать СОАС с весьма высокой степенью вероятности только лишь на основании пульсоксиметрического мониторирования.
Сатурация кислорода начинает снижаться вскоре после прекращения легочной вентиляции и обычно возвращается к исходному уровню при возобновлении дыхания. Выраженность возникающей гипоксемии зависит от длительности апноэ, объема легких, исходного насыщения крови кислородом и скорости его потребления, а при гипопноэ еще и от сохраняющегося объема вентиляции (11; 23; 25; 54). Поэтому в случае, когда легкие исходно способны обеспечить достаточный запас кислорода, короткие эпизоды апноэ и гипопноэ могут не приводить к сколько-нибудь заметной десатурации оксигемоглобина и, вследствие этого, не выявляться посредством пульсоксиметрии (53). Напротив, у пациентов с сопутствующими хроническими заболеваниями легких, значительным ожирением или альвеолярной гиповентиляцией другого генеза коротких периодов между дыхательными паузами может оказаться недостаточно для того, чтобы восстанавливать насыщение гемоглобина кислородом не только в артериальной, но и в венозной крови. В результате, хотя после возобновления дыхания сатурация кислорода продолжает возвращаться у таких больных к исходному уровню, у них наблюдается прогрессирующее нарастание глубины и скорости десатурации от одного эпизода апноэ к другому, так как в легкие возвращается все менее оксигенированная кровь (25; 54). Если же компенсаторные механизмы оказываются нарушенными в еще большей степени, у больного может возникать выраженная гипоксемия в течение всего времени сна (22; 30).
Хроническая альвеолярная гиповентиляция обычно не упоминается в числе характерных осложнений, сопровождающих СОАС. Тем не менее, гиперкапническая форма дыхательной недостаточности в состоянии бодрствования выявляется у 12-23% этих больных
(30; 33; 42). Гиповентиляция развивается в результате взаимодействия между изменениями центральных механизмов регуляции и периферическими нарушениями механики дыхания, в основе которых лежат ожирение, бронхиальная обструкция и выраженность дыхательных расстройств во время сна (12; 29; 36; 42). При этом мы показали, что у больных с гиперкапнией величина рСО2 в дневное время количественно зависит от тяжести СОАС (рис.3). У пациентов с нормальными цифрами рСО2 в бодрствовании такая зависимость не отмечается (42).
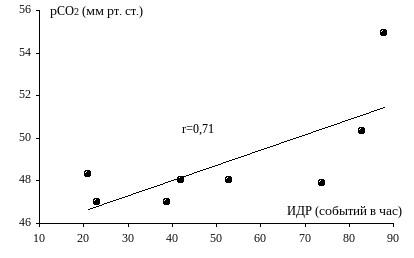 Рис. 3. Зависимость величины рСО2 от тяжести СОАС у больных с гиперкапнией в бодрствовании | Несмотря на то, что обструктивные апноэ, по всей видимости, являются независимой причиной формирования хронической дыхательной недостаточности, у большей части больных при отсутствии выраженного ожирения или хронических обструктивных заболеваний легких газы крови в состоянии бодрствования обычно остаются в пределах нормы даже при наличии достаточно тяжелого СОАС. |
Кроме того похоже, что все перечисленные факторы лишь в той или иной степени способствуют появлению хронической альвеолярной гиповентиляции у предрасположенных к этому лиц, а не предопределяют ее возникновение. Так у некоторых больных могут иметь место выраженные расстройства дыхания во время сна в сочетании с бронхиальной обструкцией и ожирением, но нет гиперкапнии в период бодрствования
(18; 42). В пользу этого же говорит и наблюдавшаяся нами только у пациентов с гиперкапнией зависимость величины рСО2 в состоянии бодрствования от тяжести СОАС.
По всей видимости, природа хронической дыхательной недостаточности у пациентов с СОАС не только является многофакторной, но и может отличаться у разных больных. Об этом свидетельствует то, что хотя хиррургическая коррекция СОАС во многих случаях приводит к повышению чувствительности к СО2, улучшению альвеолярной вентиляциии и нормализации рСО2 в состоянии бодрствования, у части пациентов положительная динамика показателей газообмена не отмечается (8; 26; 45).
СРАР-терапия позволяет более эффективно коррегировать имеющиеся у пациентов с СОАС нарушения газообмена (9; 41; 42; 61), но в этом случае механизм коррекции дыхательной недостаточности по всей видимости более сложен, так как лечение сочетает ликвидацию обструктивных апноэ во время сна с эффектом вспомогательной вентиляции легких (40). Улучшение альвеолярной вентиляции также закономерно приводит к некоторому уменьшению дневной гипоксемии у этих больных (41; 42; 51). Мы отметили (рис.4), что это происходит на фоне небольшого, но статистически достоверного улучшения показателей вентиляционной функции легких (41; 42). Впрочем, подобный эффект наблюдался не всеми авторами (51; 61).
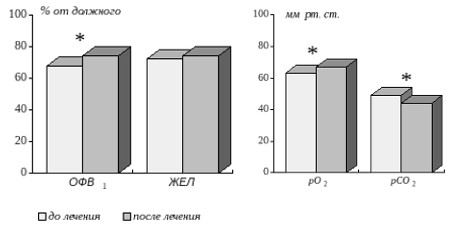
Рис. 4. Влияние лечения методом СРАР на показатели функции внешнего дыхания и газовый состав крови у больных с СОАС и хронической дыхательной недостаточностью.
Примечание: * – p <0,05.
У больных с СОАС наблюдаются циклические колебания давления в легочной артерии во время сна: оно постепенно возрастает к концу эпизода апноэ и достигает наибольшей величины после возобновлении легочной вентиляции, а затем начинает снижаться. При этом давление повышается пропорционально степени возникающей гипоксемии (34; 39). Давление заклинивания в легочных капиллярах также увеличивается (14), причем может достичь величины достаточной, чтобы вызвать отек легких у некоторых пациентов (21; 37).
Все эти изменения легочной гемодинамики, по всей видимости, представляют собой результат взаимодействия нескольких факторов, включая гипоксическую вазоконстрикцию и изменения внутригрудного давления, возникающие в результате неэффективных дыхательных попыток (34; 44; 50).
Повторяющиеся апноэ могут приводить к серьезной легочной гипертензии в течение ночи (52; 57). Повышенное давление в легочной артерии в состоянии бодрствования встречается в среднем у 20% больных с СОАС (20; 33; 49; 59), хотя в отдельных выборках легочная гипертензия наблюдается существенно чаще (5; 35; 46).
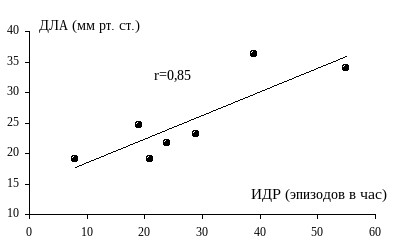 Рис. 5. Зависимость величины давления в легочной артерии от тяжести СОАС. | Хотя на сегодняшний день преобладает мнение, что повышение давления в легочной артерии в состоянии бодрствования у больных с СОАС является следствием хронических нарушений газообмена в результате бронхиальной обструкции и ожирения |
Более того, в одной из работ было показано, что наличие дневной гипоксемии не является обязательным условием ее возникновения (35).
Клинически значимая правожелудочковая недостаточность развивается у 12–27% пациентов с СОАС (6; 11; 60). Кажется маловероятным, что изолированные эпизоды ночной гипоксемии способны самостоятельно привести к правосердечной декомпенсации при отсутствии дыхательной недостаточности в дневное время. Тем не менее, хотя наличие хронических нарушений газообмена, очевидно, является обязательным условием ее возникновения (5; 11; 60), мы пришли к выводу, что обструктивные апноэ вносят свой самостоятельный вклад в возникновение правосердечной недостаточности, как за счет непосредственного влияния на легочную гемодинамику, так и опосредованно способствуя формированию хронической дыхательной недостаточности и усугубляя тем самым последствия бронхиальной обструкции и ожирения (6).
Коррекция СОАС предотвращает ночные повышения давления в легочной артерии (57). Нормализация дыхания во время сна в ряде случаев вызывает снижение легочного артериального давления и в состоянии бодрствования (5; 8; 38). Однако этот эффект отмечается не у всех пациентов (5; 51). Более того, на фоне СРАР-терапии легочное артериальное давление в ряде случаев даже умеренно увеличивается (5), хотя нельзя однозначно сказать, носит ли это явление негативный характер или, напротив, отражает улучшение сократительной функции правого желудочка.
При наличии дисфункции правого желудочка устранение СОАС приводит к увеличению его фракции выброса (13; 47), что у части пациентов с клиникой правосердечной недостаточности позволяет добиться уменьшения или даже полного исчезновения периферических отеков без дополнительной медикаментозной терапии (41; 56). Впрочем, предсказать подобный эффект на практике затруднительно, а его наличие с нашей точки зрения не позволяет подменять медикаментозную терапию сердечной недостаточности только лечением расстройств дыхания во время сна.
Сочетание обструктивного апноэ с хроническими обструктивными заболеваниями легких получило название синдрома “перекреста” (24), являющегося по своей сути синдромом взаимного отягощения. Подобная комбинация наблюдается в среднем у 11-13% больных с СОАС (4; 19), но может встречаться и чаще в зависимости от особенностей выборки (41).
Наличие двух различных этиологических факторов предрасполагает к более тяжелой дыхательной недостаточности. В результате хроническая легочная гипертензия и правожелудочковая сердечная недостаточность возникают у них существенно чаще и в более ранние сроки, чем если бы они имели только одно из этих патологических состояний, несмотря на то, что некоторые из них имеют относительно мало измененные показатели вентиляционной функции легких (4; 5; 19; 59; 60). Кроме того у больных с ночными приступами бронхиальной астмы именно эпизоды обструктивного апноэ могут оказаться тем фактором, который и провоцирует возникновение бронхиальной обструкции во время сна (3; 17).
Имеющиеся при СОАС нарушения газообмена вызывают изменения свободнорадикального гомеостаза, проявляющиеся в виде дефицита активных форм кислорода и активации перикисного окисления липидов (1, 2). Вероятно, эти сдвиги свободнорадикальных процессов также могут играть определенную роль в патогенезе различных сердечно-сосудистых нарушений, развивающихся у больных с расстройствами дыхания во время сна.
Отражением формирующейся дыхательной недостаточности является вторичный эритроцитоз, который может развиться у пациентов с СОАС даже при отсутствии хронических заболеваний легких и приводит к нарушению реологических свойств крови, повышая риск возникновения различных сосудистых катастроф (27).
Подводя итоги всего сказанного выше, вероятный патогенез имеющихся у больных с СОАС хронических расстройств газообмена и легочной гемодинамики можно условно представить в виде следующей схемы (рис.5).
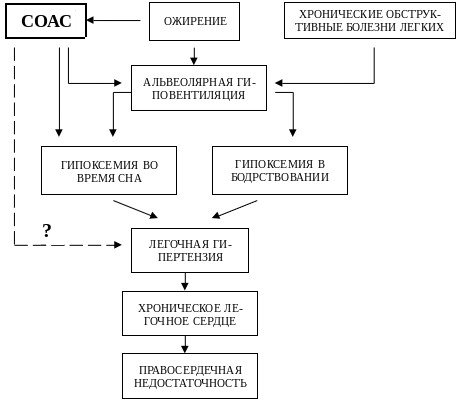
Рис. 6. Вероятные механизмы патогенеза хронических нарушений газообмена и легочной гемодинамики у больных с СОАС.
Таким образом, легочная гипертензия и правосердечная недостаточность у больных с СОАС, по всей видимости, возникают как следствие нарушений газообмена, развивающихся в результате взаимодействия между обструктивными апноэ, ожирением и тяжестью имеющейся бронхолегочной патологии
Несмотря на некоторую противоречивость имеющихся на сегодняшний день мнений, основываясь на результатах собственных исследований и данных литературы, мы приходим к выводу о том, что СОАС является не только самостоятельной, но и весьма значимой причиной различных кардиореспираторных расстройств. Осознание этого факта имеет не столько научное, сколько большое практическое значение. Необходимо понимать, что симптоматическое лечение имеющихся у таких пациентов нарушений дыхания и гемодинамики часто оказывается недостаточно эффективным и не может подменять собой патогенетическую терапию, направленную на непосредственную коррекцию СОАС.
ЛИТЕРАТУРА
- Ан Г. В., Даниляк И.Г., Коган А.Х., Болевич С. К вопросу об ингибирующем влиянии СО2 на свободнорадикальные процессы у больных с синдромом апноэ во сне //
9 национальный конгресс по болезням органов дыхания: Сборник резюме. – М., 1999. – С.328. - Ан Г. В., Пальман А. Д., Коган А. Х. Перикисное окисление липидов у больных с синдромом апноэ во сне // 9 национальный конгресс по болезням органов дыхания: Сборник резюме. – М., 1999. – С.328.
- Бейтуганова Е. О., Чучалин А. Г., Колганова Н. А. и др. Роль рефлюкс-эзофагита и синдрома апноэ во сне в генезе ночных приступов удушья // Пульмонология. – 1998. – №2. – С.53-58.
- Белов А. М. Обструктивные нарушения во время сна: методологические основы диагностики, синдром “перекреста”, кардиоваскулярные проявления: Дис. ... д-ра. мед. наук. – М., 1998.
- Пальман А. Д. Давление в легочной артерии у больных с синдромом апноэ во сне и его динамика в процессе лечения: Дис. ... канд. мед. наук. – М., 1997.
- Пальман А. Д. К вопросу о патогенезе правосердечной недостаточности у больных с синдромом обструктивного апноэ во сне // Актуальные проблемы сомнологии: Тезисы докладов Всероссийской конференции. – М., 1998. – С.76.
- Пальман А. Д., Учкина Е. А. Информативность результатов исследования функции внешнего дыхания у больных с синдромом апноэ во сне // Сборник научных трудов кафедры внутренних болезней №2 первого лечебного факультета и клиники госпитальной терапии им. А. А. Остороумова. – М., 1998. – С.75-77.
- Aubert-Tulkens G., Willems B., Veriter C. et al. Increase in ventilatory response to CO2 following tracheostomy in obstructive sleep apnea // Bull. Eur. Physiopathol. Respir. – 1980. – Vol.16, №5. – P.587-593.
- Berton-Jones M., Sullivan C. E. Time course of change in ventilatory response to CO2 with long-term CPAP therapy for obstructive sleep apnea // Am. Rev. Respir. Dis. – 1987. – Vol.135, №1. – P.144-147.
- Bradley T. D., Martinez D., Rutherford R. et al. Physiological determinants of nocturnal arterial oxygenation in patients with obstructive sleep apnea // J. Appl. Physiol. – 1985. – Vol. 59., №5 – P. 1364-1368.
- Bradley T. D., Rutherford R., Grossman R. F. et al. Role of day-time hypoxemia in the pathogenesis of right heart failure in the obstructive sleep apnea syndrome // Am. Rev. Respir. Dis. – 1985. – Vol.131, №6. – P.835-839.
- Bradley T. D., Rutherford R., Lue F. et al. Role of diffuse airway obstruction in the hypercapnia of obstructive sleep apnea // Am. Rev. Respir. Dis. – 1986. – Vol.134, №5. – P.920-924.
- Bradley T. D. Right and left ventricular impairment and sleep apnea // Clin. Chest Med. – 1992. – Vol.13, №3. – P. 459-479.
- Buda A. J., Schroeder J. S., Guilleminault C. Abnormalities of pulmonary artery wedge pressure in sleep-induced apnea // Int. J. Cardiol. – 1981. – Vol.1. – P.67-74.
- Burwell C. S., Robin E. D., Whaley R. D., Bickelmann A. G. Extreme obesity associated with alveolar hypoventilation – a Pickwickian syndrome // Am. J. Med. – 1956. – Vol.21, №5. – P.811-818.
- Campbell A.H., Guy P.A., Rochford P.D. et al. Flow-volume curve changes in patients with obstructive sleep apnoea and brief upper airway dysfunction // Respirology. – 2000. – Vol.5, №1 – P.11-18.
- Chan C. S., Woolcock A. J., Sullivan C. E. Nocturnal asthma: Role of snoring and sleep apnea // Am. Rev. Respir. Dis. – 1988. – Vol.137. – P.1502-1504.
- Chan C. S., Grunstein R. R., Bye P. T. et al. Obstructive sleep apnea with severe chronic airflow limitation. Comparison of hypercapnic and eucapnic patients // Am. Rev. Respir. Dis. – 1989. – Vol.140, №5. – P.1274-1278.
- Chaouat A., Weitzenblum E., Krieger J. et al. Association of chronic obstructive pulmonary disease and sleep apnea syndrome // Am. J. Respir. Crit. Care Med. – 1995. – Vol.151, №1. – Р.82-86.
- Chaouat A., Weitzenblum E., Krieger J. et al. Pulmonary haemodynamics in the obstructive sleep apnea syndrome. Results in 220 consecutive patients // Chest. – 1996. – Vol. 109, №2. – P.380-386.
- Chaudhary B. A., Nadimi M., Chaudhary T.K., Speir W.A. Pulmonary edema due to obstructive sleep apnea // South. Med. J. – 1984. – Vol.77, №4. – Р.499-501.
- Douglas M. J. Breathing during sleep in patients with chronic obstructive pulmonary disease // Principles and Practise of Sleep Medicine. – 2-nd Ed. – Philadelphia: Harcourt Brace & Company, 1994. – P.758-768.
- Findley L. J., Ries A. L., Tisi G. M. et al. Hypoxemia during apnea in normal subjects: mechanisms and impact of lung volume // J. Appl. Physiol. – 1983. – Vol. 55. – P.1777-1783.
- Flenley D. S. Sleep in chronic obstructive lung disease // Clin. Chest. Med. – 1985. – Vol.6, №4. – P. 651-661.
- Fletcher E. C. Central venous oxygen saturation, abnormal gas exchange and rate of fall of arterial oxyhemoglobin saturation during obstructive sleep apnea // Sleep and Health Risk. – Berlin: Springer, 1991. – P.183-192.
- Gislason T., Tammivaara R. Airway obstruction, obesity and CO2 ventilatory responsiveness in the sleep apnea syndrome // Ups. J. Med. Sci. – 1992. – Vol.97, №2. – P.141-148.
- Guilleminault C. Clinical features and evaluation of obstructive sleep apnea // Principles and Practice of Sleep Medicine. – 2-nd Ed. – Philadelphia: Harcourt Brace & Company, 1994. – P. 667-677.
- Haponik E.F., Bleeker E.R., Allen R.P. et al. Abnormal inspiratory flow-volume curves in patients with sleep-disordered breathing // Am. Rev. Respir. Dis. – 1981. – Vol.124, №5. – P.571-574.
- Javaheri S., Colangelo G., Lacey W., Gartside P. S. Chronic hypercapnia in obstructive sleep apnea-hypopnea syndrome // Sleep. – 1994. – Vol.17, №5. – P.416-423.
- Jones J. B., Wilhoit S. C., Findley L. J. et al. Oxyhemoglobin saturation during sleep in patients with and without the obesity-hypoventilation syndrome // Chest. – 1985. – Vol.88, №1. – P.9-15.
- Katz I., Zamel N., Slutsky A.S. et al. An evaluation of flow-volume curves as a screening test for obstructive sleep apnea // Chest. – 1990. – Vol.98, №2. – P.337-340.
- Krieger J., Weitzenblum E., Vandevenne A. et al. Flow-volume curve abnormalities and obstructive sleep apnea syndrome // Chest. – 1985. – Vol.87, №2. – P.163-167.
- Krieger J., Sforza E., Apprill M. et al. Pulmonary hypertension, hypoxemia and hypercapnia in obstructive sleep apnea patients // Chest. – 1989. – Vol.96, №4. – P.729-737.
- Krieger J., Weitzenblum E. Pulmonary hemodynamics in the obstructive sleep apnea syndrome // Sleep and Health Risk. – Berlin: Springer, 1991. – P.356-370.
- Laks L., Lehrhaft B., Grunstein R. R., Sullivan C. E. Pulmonary hypertension in obstructive sleep apnea // Eur. Respir. J. – 1995. – Vol. 8, №4. – P.537-541.
- Leech J. A., Onal E., Baer P., Lopata M. Determinants of hypercapnia in occlusive sleep apnea syndrome // Chest. – 1987. – Vol.92. – P.807.
- Liam C. K., Liao C. M., Kannan P. Recurrent acute pulmonary oedema associated with obstructive sleep apnoea // Singapore Med. J. – 1994. – Vol.35, №4. – Р.411-413.
- Lugaresi E., Coccagna G., Mantovani M., Brignani F. Effect of tracheostomy in two cases of hypersomnia with periodic breathing // J. Neurol.- 1973.- Vol. 36, №1.- P. 15 - 26.
- Marrone O., Bellia U., Ferrara G. et al. Transmural pressure measurements. Importance in the assessment of pulmonary hypertension in obstructive sleep apneas // Chest. – 1989. – Vol.95, №2. – P.338-344.
- Miro A. M., Shivaram U., Hertig I. Continuous positive airway pressure in COPD patients in acute hypercapnic respiratory failure // Chest. – 1993. – Vol.103, №1. – P.266-268.
- Palman A. D., Danilyak I. G., Eligulashvili T. S., Roitman E. V. The effect of treatment with continuous positive airway pressure on lung function in patients with sleep apnea syndrome // Somnologie. – 1997. – №1, Suppl.2. – P.45.
- Palman A. D., Roitman E. V., Danilyak I. G. Daytime respiratory failure in patients with obstructive sleep apnea and it’s treatment with continuous positive airway pressure // Sleep Research Online. – 1999. – Vol.2., Suppl.1. – P. 417.
- Peter J.H., Köhler U., Grote L., Podszus T. Manifestation and consequences of obstructive sleep apnoea // Eur. Respir. J. – 1995. – Vol.8. – P. 1572-1583.
- Podszus T., Mayer J., Penzel T. et al. Nocturnal hemodynamics in patients with sleep apnea // Eur. J. Respir. Dis. – 1986. – Vol.69. – P.435-442.
- Rapoport D. M., Garay S. M., Epstein H., Goldring R. M. Hypercapnia in the obstructive sleep apnea syndrome. A reevaluation of the "Pickwickian syndrome" // Chest. – 1986. – Vol.89, №5. – P.627-635.
- Sajkov D., Cowie R. J., Thornton A. T. et al. Pulmonary hypertension and hypoxemia in obstructive sleep apnea syndrome // J. Respir. Crit. Care Med. – 1994. – Vol.149, №2. –
P. 416-422. - Sanchez V.A., Gil C.F., Ruiz R.A. et al. Efecto de la presion positiva continua en la via aerea a traves de la nariz sobre la function ventricular derecha en el sindrome de apnea obstructiva del sueno // Med. Clin. Barc. – 1993. – Vol.101, №4. – P.128-131.
- Sanders M.H., Martin R.J., Pennock B.E., Rogers R.M. The detection of sleep apnea in the awake patient. The “saw-tooth” sign // JAMA. – 1981. – Vol.245, №23. – P.2414-2418.
- Sanner B. M., Doberauer C., Konermann M. et al. Pulmonary hypertension in patients with obstructive sleep apnea syndrome // Arch. Intern. Med. – 1997. – Vol.157, №21. –
Р. 2483-2487. - Schafer H., Hasper E., Ewig S. et al. Pulmonary haemodynamics in obstructive sleep apnoea: time course and associated factors // Eur. Respir. J. – 1998. – Vol.12, №3. – P.679-684.
- Sforza E., Krieger J., Weitzenblum E. et al. Long-term effects of treatment with nasal continuous positive airway pressure on daytime lung function and pulmonary hemodynamics in patints with obstructive sleep apnea // Am. Rev. Respir. Dis., 1990. – Vol.141, №4. – P.866-870.
- Sforza E., Laks L., Grunstein R.R. et al. Time course of pulmonary artery pressure during sleep in sleep apnoea syndrome: role of recurrent apnoeas // Eur. Respir. J. – 1998. – Vol.11, №2. – P.440-446.
- Shepard J. W., Staats B. A. Trend oximetry // Atlas of Sleep Medicine. – New York: Futura Publishing Company, 1991. – P.159-170.
- Shepard J. W. Cardiorespiratory changes in obstructive sleep apnea // Principles and Practice of Sleep Medicine. – 2-nd Ed. – Philadelphia: Harcourt Brace & Company, 1994. – P. 657-666.
- Shinozaki T., Tatsumi K., Sakuma T. et al. Daytime pulmonary hypertension in the obstructive sleep apnea syndrome // Nihon Kyobu Shikkan Gakkai Zasshi. – 1995. – Vol.33, №10. – P.1073-1079.
- Sullivan C. E., Grunstein R. R. Continuous positive airway pressure in sleep-disordered breathing // Principles and Practise of Sleep Medicine. – 2-nd Ed. – Philadelphia: Harcourt Brace & Company, 1994. – P.694-705.
- Thalhofer S., Kaufmann U., Dorow P. Veranderung der Hamodynamik mit und ohne CPAP-Beatmung bie Patienten mit Schlafapnoesyndrom // Pneumologie. – 1991. – Bd.45, Suppl.1. – S.293-295.
- Vincken W., Cosio M.G. Flow oscillations on the flow-volume loop: a nonspecific indicator of upper airway dysfunction // Bull. Eur. Physiopathol. Respir. – 1985. – Vol. 21, №6. –
P.559-567. - Weitzenblum E., Krieger J, Apprill M. et al. Daytime pulmonary hypertension in patients with obstructive sleep apnea syndrome // Am. Rev. Respir. Dis. – 1988. – Vol.138, №2. –
Р.345-349. - Whyte K.F., Douglas N.J. Peripheral edema in the sleep apnea/hypopnea syndrome // Sleep. – 1991. – Vol.14, №4. – Р.354-356.
- Young I. H., Mihalyka M., Costas L., Sullivan C. E. Long term lung function changes in patients with obstructive sleep apnea during treatment with nasal continuous positive airway pressure// Thorax. – 1987. – Vol. 42. – P. 722.
