Эффективное лечение хронической дыхательной недостаточности, связанной с морбидным ожирением
Известно, что значительный избыток веса может стать причиной хронической дыхательной недостаточности – так называемого синдрома ожирения-гиповентиляции, исторически также упоминающегося в литературе как синдром Пиквика (1). Под этим термином понимается патологическое состояние, при котором у больного с морбидным ожирением развивается хроническая альвеолярная гиповентиляция – гиперкапническая дыхательная недостаточность (РаСО2> 45 мм рт. ст.), которую нельзя объяснить никакими другими причинами, кроме значительного избытка веса (2). Кроме того, у большинства таких пациентов одновременно наблюдаются тяжелые нарушения дыхания во время сна (3), что позволяет ряду авторов рассматривать обструктивное апноэ сна в качестве одной из важных составляющих Пиквикского синдрома (4). При этом хроническая дыхательная недостаточность, как исход выраженного ожирения не является чем-то редким и по данным D. D. Sin et al. (2000) развивается у трети таких больных (5). Патофизиологические механизмы, приводящие к возникновению синдрома ожирения-гиповентиляции, все еще дискутируются в литературе и по всей видимости представляют собой сочетание рестриктивных нарушений легочной вентиляции, хронического утомления дыхательной мускулатуры и нарушения центральных механизмов регуляции дыхания (6). При этом наиболее выраженными дыхательные нарушения оказываются во время сна. Это объясняется дальнейшим ухудшением механики дыхания в положении лежа за счет давления абдоминального жира на диафрагму, а также естественным снижением тонуса дыхательных мышц и понижением центрального респираторного ответа на гипоксемию и гиперкапнию в состоянии сна (7). Присоединение обструктивного апноэ сна еще больше усугубляет тяжесть наблюдающихся у таких пациентов дыхательных расстройств.
До сегодняшнего пациент с синдромом ожирения-гиповентиляции представляет для отечественных практических врачей определенную проблему. Дело в том, что эффективной и безопасной медикаментозной терапии этого состояния не найдено, снижение веса может привести к положительным сдвигам лишь в долгосрочной перспективе, а необдуманное назначение малопоточной кислородотерапии для коррекции гипоксемии, обычно наблюдающейся у таких больных, может привести к еще большему угнетению дыхания и нарастанию гиперкапнии (8). Однако на сегодняшний день мы имеем возможность эффективно лечить таких больных, что наглядно иллюстрирует следующее клиническое наблюдение.
 Рис. 1. Пациентка С., 52 лет, индекс массы тела 58 кг/м2. | Пациентка С, 52 лет (рис. 1.), бухгалтер, была госпитализирована в кардиологическое отделение Университетской клинической больницы №1 Первого МГМУ им. И.М. Сеченова в феврале 2016 г. При поступлении предъявляла жалобы на одышку при небольших физических нагрузках, таких как спокойная ходьба на расстояние 100-200 м., выраженную дневную сонливость, слабость, быструю утомляемость, беспокойный прерывистый сон, головные боли – преимущественно утром после пробуждения. Из анамнеза известно, что с детства была предрасположена к избыточному весу. В возрасте 20 лет во время первой беременности впервые стала отмечать умеренное повышение артериального давления. После вторых родов в возрасте 37 лет за короткое время прибавила в весе около 40 кг, тогда же стала отмечать беспокоящий окружающих громкий храп, появилась дневная сонливость, начала беспокоить одышка при повседневных физических нагрузках, таких как работа по дому. |
Приблизительно в это же время отмечено прогрессирование артериальной гипертонии с максимальными цифрами артериального давления до 220/110 мм рт. ст., несмотря на регулярный прием гипотензивных препаратов. В 2010 г. у пациентки диагностирован синдром обструктивного апноэ сна (СОАС), но на тот момент от рекомендованной СиПАП-терапии она отказалась. Ухудшение состояния с лета 2015 г., когда больная отметила прогрессирующее снижение толерантности к физическим нагрузкам и нарастание сонливости – стали возникать эпизоды приступообразного засыпания, что периодически приводило к падениям и ушибам.
При поступлении в клинику состояние средней тяжести. Питание значительно повышено – индекс массы тела 58 кг/м2. Цианоз губ. Частота дыхания 20-22 в минуту. Измеренная с помощью пульсоксиметра сатурация кислорода в покое – 92%, при ходьбе снижается до 88%. Над легкими дыхание ослаблено, хрипы не выслушиваются. Из-за выраженного ожирения границы сердечной тупости не определяются. Тоны сердца приглушены, ритм правильный с частотой сердечных сокращений 90 в мин., патологические шумы не выслушиваются. Артериальное давление 210/100 мм рт. ст. на фоне терапии тремя гипотензивными препаратами в адекватных дозах. Живот значительно увеличен в объеме за счет жировой клетчатки, при пальпации мягкий, безболезненный. Печень и селезенка не пальпируются. Симптом поколачивания по поясничной области отрицательный, дизурии нет. Голени отечны. Грубой неврологической симптоматики нет.
Результаты лабораторного и инструментального обследования:
В общем анализе крови: гемоглобин 136 г/л, эритроциты 4.9 х 1012/л, цветовой показатель 0.82, тромбоциты 149 х 109/л; лейкоциты 7.4х109/л, лейкоцитарная формула без особенностей, СОЭ 14 мм/ч. В биохимическом анализе крови отмечена тенденция к незначительному повышению уровня глюкозы натощак, а в остальном также без существенных патологических отклонений. Гормоны щитовидной железы в норме. При исследовании КЩС и газового состава крови: PaО2 – 61 мм рт. ст., PaСО2 – 52 мм рт. ст., компенсированный дыхательный ацидоз.
На ЭКГ синусовый ритм с частотой сердечных сокращений 83 в минуту, признаки гипертрофии левого желудочка. Отрицательные зубцы Т в III и AVF отведениях, возвращающиеся к изолинии при повторной регистрации ЭКГ на вдохе.
Эхокардиографическое исследование выявило дилатацию левого и правого предсердий, умеренную гипертрофию миокарда левого желудочка, а также незначительную регургитацию на митральном и трехстворчатом клапанах. Показатели систолической функции левого желудочка оставались в пределах нормы. Диастолическая функция также существенно не нарушена. Вызывало определенные вопросы отсутствие гипертрофии миокарда правого желудочка и признаков легочной гипертензии у пациентки с хронической дыхательной недостаточностью. Однако, с учетом объективной трудности выполнения ультразвукового исследования сердца при морбидном ожирении полученные результаты вполне могут быть ложно отрицательными.
Суточное мониторирование ЭКГ не выявило клинически значимых нарушений сердечного ритма и проводимости, а также признаков ишемии миокарда.
При рентгеновском исследовании органов грудной клетки очаговые и инфильтративные изменения не выявлены, признаков венозного застоя в малом круге кровообращения нет. Обращает на себя внимание увеличение тени сердца преимущественно за счет его левых отделов.
По данным ультразвукового исследования органов брюшной полости печень нормальных размеров, без признаков венозного застоя. Почки не изменены.
Исследование функции внешнего дыхания показало наличие умеренных вентиляционных нарушений по рестриктивному типу.
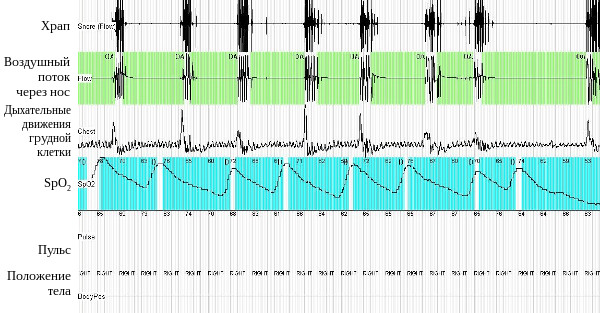
Рис. 2. Респираторное мониторирование во время сна у больной С. (фрагмент записи). Регистрируются множественные эпизоды обструктивного апноэ. Исчезновение дыхательного потока происходит на фоне сохраняющихся дыхательных усилий и сопровождается значительным снижением SрO2. При возобновлении легочной вентиляции возникает храп.
Больной было проведено респираторное мониторирование во время сна, выявлены множественные эпизоды апноэ и гипопноэ обструктивного характера (рис. 2). Индекс апноэ-гипопноэ – 93 события в час. Минимальная сатурация во время сна 50% при средней сатурации 66%. Обращало на себя внимание, что даже при отсутствии эпизодов апноэ и гипопноэ сатурация кислорода во время сна оставалась крайне низкой – порядка 86-87% (рис. 3.). Сделано заключение о наличии у пациентки синдрома обструктивного апноэ сна тяжелого течения и синдрома ожирения-гиповентиляции.
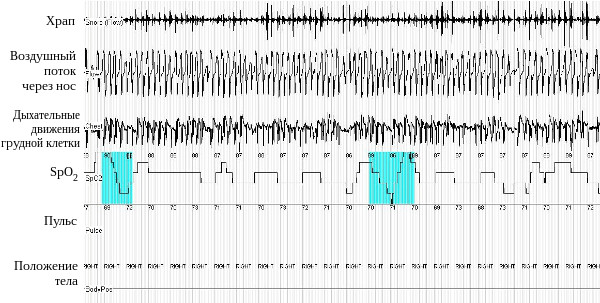
Рис. 3. Респираторное мониторирование во время сна у больной С. (фрагмент записи). Даже при отсутствии эпизодов апноэ наблюдается стойкая гипоксемия со снижением SрO2 до 86-87%. Наличие регулярного храпа косвенно подтверждает, что пациентка в этот момент спит.
Консультация сосудистого хирурга: Хроническая венозная недостаточность.
Консультация эндокринолога: Нарушение толерантности к глюкозе.
Анализ результатов проведенного обследования позволил исключить кардиогенную природу одышки. Было сделано заключение о том, что пациентка с тяжелой артериальной гипертонией и с морбидным ожирением, также страдает синдромом обструктивного апноэ сна тяжелого течения и синдромом ожирения-гиповентиляции (Пиквикский синдром) с формированием хронической дыхательной недостаточности. С учетом того, что нарушения газообмена были в значительной мере ассоциированы со сном и в меньшей степени проявлялись во время бодрствования, наряду с коррекцией гипотензивной терапии пациентке был начат подбор режима вспомогательной вентиляции во время ночного сна. На фоне начатой СиПАП-терапии удалось устранить эпизоды обструкции верхних дыхательных путей, но явления альвеолярной гиповентиляции при этом сохранялись – средняя сатурация кислорода во время сна составила 87%. Соответственно следующим этапом стало начало неинвазивной вспомогательной вентиляции легких с двумя уровнями положительного давления – БиПАП, также только во время ночного сна. При этом величина давления выдоха была установлена согласно оттитрованной раньше величине СиПАП, что гарантировало пациентке беспрепятственную вентиляцию верхних дыхательных путей. Давление вдоха увеличивалось постепенно вплоть до достижения целевой сатурации кислорода более 90%, что в итоге позволило полностью компенсировать имевшие место дыхательные нарушения во время сна.
В результате проводимого лечения состояние пациентки значительно улучшилось: нормализовался сон, перестали беспокоить головные боли по утрам, исчезла дневная сонливость, ощутимо повысилась переносимость физических нагрузок – больная смогла без одышки ходить в пределах отделения. На фоне неинвазивной респираторной поддержки средняя сатурация кислорода во время сна составила 92%. Спустя 1 неделю от начала лечения частота дыхания днем в покое – 18 в минуту, а SpO2 при пульсоксиметрии – 94% и не снижается ниже 90% при спокойной ходьбе. Одновременно было отмечено восстановление чувствительности к гипотензивным препаратам – на фоне терапии эналаприлом, амлодипином и индапамидом достигнута стойкая стабилизация артериального давления на уровне 140/80 мм рт. ст. При контрольном исследовании газового состава артериальной крови в бодрствовании гиперкапния полностью купирована: РаО2 – 66 мм рт. ст. и РаСО2 – 43 мм рт. ст.
В результате больной был поставлен следующий клинический диагноз:
Основное заболевание: Артериальная гипертония 2 стадии, 3 степени, риск IV.
Сочетанные заболевание: Синдром ожирения-гиповентиляции. Синдром обструктивного апноэ сна тяжелого течения.
Фоновые заболевания: Ожирение 3 ст. Нарушение толерантности к глюкозе.
Осложнения: Вентиляционные нарушения 1 ст. по рестриктивному типу. Хроническая дыхательная недостаточность 2 ст.
Выписана через 2 недели пребывания в стационаре в удовлетворительном состоянии с рекомендациями продолжить неинвазивную вспомогательную вентиляцию легких в режиме БиПАП во время ночного сна, прием гипотензивных препаратов в подобранных дозах, а также низкокалорийную диету для снижение веса.
Таким образом, на сегодняшний день применение неинвазивной вспомогательной вентиляции легких является методом выбора при лечении больных с синдромом ожирения-гиповентиляции (рис. 4) и полностью соответствует патофизиологической логике гиперкапнической дыхательной недостаточности, позволяя снизить нагрузку на дыхательную мускулатуру, оптимизировать механику дыхания и восстановить чувствительность дыхательного центра к СО2 (9), одновременно обеспечивая проходимость верхних дыхательных путей во время сна. Благодаря создаваемому резерву это в целом ряде случаев позволяет задействовать вспомогательную вентиляцию прерывисто – только во время ночного сна, в то время как в бодрствовании пациент оказывается способен самостоятельно поддерживать адекватный уровень газообмена.
У пациентов с тяжелым СОАС и умеренными нарушениями газообмена в течении дня лечение следует начинать с СиПАП-терапии – дыхания с постоянным положительным давлением воздуха, что позволяет устранить обструкцию верхних дыхательных путей во время сна. Однако резвившаяся на фоне обструктивного апноэ сна хроническая дыхательная недостаточность по всей видимости отличается по своей природе у разных пациентов. В пользу этого свидетельствует тот факт, что коррекция СОАС приводит к улучшению альвеолярной вентиляции и нормализации показателей газообмена в состоянии бодрствования лишь у части пациентов, в то время как у других положительная динамика показателей газообмена не отмечается (10). Это позволяет клинически разделять пациентов с СОАС и хронической гиперкапнией на подгруппы с апноэ-зависимым и апноэ-независимым и механизмами развития альвеолярной гиповентиляции. И если в первом случае коррекции СОАС бывает достаточно для нормализации показателей газообмена и в бодрствовании, то во втором требуются дополнительные терапевтические опции. Однако так как предсказать заранее к какой из перечисленных групп относится тот или иной пациент до начала лечения затруднительно, то терапия синдрома ожирения-гиповентиляции должна начинаться с устранения обструктивных нарушений дыхания во время сна.
Если СиПАП-терапия не привела к нормализации РаСО2 и устранению гипоксемии во время сна, когда исходная тяжесть дыхательной недостаточности велика или СОАС изначально отсутствует, то пациенту показана классическая неинвазивная вентиляция. Вспомогательная вентиляция подразумевает, что подача аппаратных вдохов производится с учетом самостоятельных дыхательных попыток пациента и синхронизирована с ними. Наибольшее распространение для использования вне палат интенсивной терапии в нашей стране получили портативные аппараты для неинвазивной респираторной поддержки в режиме контроля по давлению – БиПАП. При этом давление выдоха устанавливается на уровне, позволяющем поддерживать верхние дыхательные пути в открытом состоянии, т.е. по сути соответствует величине давления СиПАП, после чего постепенно повышается давление вдоха до величины, позволяющей устранить гиповентиляцию и добиться сатурации кислорода более 90%. Если целевой величины SpO2 достигнуть не удается, то на следующем этапе к лечению следует добавить кислород (6).
![Алгоритм подбора респитаторной терапии при синдроме ожирения-гиповентиляции [по Al Dabal L. et al. (2009) с изменениями] (12). Алгоритм подбора респитаторной терапии при синдроме ожирения-гиповентиляции [по Al Dabal L. et al. (2009) с изменениями] (12).](/images/algoritm-podbora-respiratornoj-terapii.jpg)
Рис. 4. Алгоритм подбора респитаторной терапии при синдроме ожирения-гиповентиляции [по Al Dabal L. et al. (2009) с изменениями] (12).
ЛИТЕРАТУРА:
- Burwell C.S., Robin E.D., Whaley R.D. et al. Extreme obesity associated with alveolar hypoventilation: A Pickwickian syndrome // Am. J. Med. – 1956. – Vol.21. – P.811-818.
- Olson A.L., Zwillich C. The obesity hypoventilation syndrome // Am. J. Med. – 2005. – Vol.118. – P.948-956.
- Randerath W.J., Stieglitz S., Galetke W. et al. Pathophysiology of the obesity hypoventilation syndrome // Pneumologie. – 2008. – Vol.62. – P.398-403.
- Berger K.I., Ayappa I., Chatr-Amontri B. et al. Obesity hypoventilation syndrome as a spectrum of respiratory disturbances during sleep // Chest. – 2001. – Vol.120. – P.1231–1238.
- Sin D.D., Jones R. L., Man G.C. Hypercapnic ventilatory response in patients with and without obstructive sleep apnea: do age, gender, obesity, and daytime PaCO2 matter? // Chest. – 2000. – Vol.117. – P.454-459.
- Shetty S., Parthasarathy S. Obesity hypoventilation syndrome // Curr. Pulmonol. Rep. – 2015. – Vol.4. – P.42-55.
- Böing S., Randerath W. J. Chronic hypoventilation syndromes and sleep-related hypoventilation // J. Thorac. Dis. – 2015. – Vol. 7. – P.1273-1285.
- Hollier C.A., Harmer A.R., Maxwell L.J. et al. Moderate concentrations of supplemental oxygen worsen hypercapnia in obesity hypoventilation syndrome: a randomised crossover study // Thorax. – 2014. – Vol.69. – P.346-353.
- Elliott M., Nava S., Schonhofer B. Non-invasive Ventilation and Weaning: Principles and Practice. – Edward Arnold Publishers Ltd., 2010. – P.228-235.
- Пальман А. Д. Функция внешнего дыхания, газообмен и легочная гемодинамика у больных с синдромом обструктивного апноэ во сне // Синдром апноэ во сне и другие расстройства дыхания, связанные со сном: клиника, диагностика, лечение. – М.: Эйдос Медиа, 2002. – С. 213-223.
- Батурова В.Ю., Малявин А.Г., Пальман А.Д. Домашняя неинвазивная вентиляция легких у больных с хронической гиперкапнической дыхательной недостаточностью // Клиническая геронтология. – 2015. – №11-12. – С. 33-38.
- Al Dabal L., BaHammam A.S. Obesity hypoventilation syndrome // Ann. Thorac. Med. – 2009. – Vol.4. – P. 41-49.
