Сомнологический кабинет
УНИВЕРСИТЕТСКОЙ КЛИНИЧЕСКОЙ БОЛЬНИЦЫ № 1ПЕРВОГО МОСКОВСКОГО ГОСУДАРСТВЕННОГО МЕДИЦИНСКОГО УНИВЕРСИТЕТА им. И. М. Сеченова
+7 (495) 178-01-04
+7 (915) 432-96-50
Заказать звонокТолько Москва и Моск. область
Диагностика и лечение синдрома обструктивного апноэ сна в амбулаторной практике
Согласно «Международной классификации расстройств сна» (2014) выделяют несколько вариантов нарушений дыхания во время сна, различных по своей этиологии и клиническим проявлениям. Это синдром обструктивного апноэ сна (СОАС), синдромы центрального апноэ сна, включая дыхание Чейна-Стокса, гиповентиляция и гипоксемия во время сна. При этом СОАС является не только самым распространенным из перечисленных выше, но, принимая во внимание его последствия, одним из наиболее значимых с клинической точки зрения патологических состояний, непосредственно связанных со сном.
СОАС характеризуется повторными эпизодами полной или частичной окклюзии верхних дыхательных путей (обструктивными апноэ и гипопноэ), которые вызывают нарушение нормальной структуры сна и часто сопровождаются снижением насыщения крови кислородом.
Происходящие у пациента с СОАС во время сна процессы схематично можно представить следующим образом. После засыпания мышечный тонус понижается. Мышцы, отвечающие за поддержание глотки в стабильном состоянии, расслабляются, и стенки верхних дыхательных путей начинают колебаться и вибрировать в проходящем через них при дыхании воздушном потоке. Периодически амплитуда таких колебаний оказывается столь велика, что происходит значительное или даже полное смыкание стенок глотки. В результате, не смотря на сохраняющиеся дыхательные движения, воздух в легкие поступает в недостаточном количестве или не попадает вовсе, нарастает гипоксемия. Это и есть обструктивные гипопноэ и апноэ. Чтобы восстановить нормальную легочную вентиляцию необходимо повысить тонус стенок верхних дыхательных путей, а для этого нужно проснуться. В итоге происходит активация мозга, которая представляет собой не полное пробуждение, а лишь переход на несколько секунд в состояние дремоты. Однако мышечный тонус успевает возрасти, а вместе с ним восстанавливается проходимость глотки. Пациент начинает нормально дышать, погружается в сон, мышечный тонус снова падает и описанный цикл патологических событий повторяется вновь. В результате множества микропробуждений нормальная структура сна оказывается грубо нарушена, он становится фрагментированным и поверхностным.
Выраженность имеющихся у пациента дыхательных расстройств оценивают на основании так называемого индекса апноэ-гипопноэ – среднего числа патологических дыхательных событий за час сна (табл. 1).
Таблица 1. Классификация СОАС на основании индекса апноэ-гипопноэ
[AASM Task Force, 1999].
| Тяжесть СОАС | Норма | Легкий | Средней тяжести | Тяжелый |
| Индекс апноэ-гипопноэ | менее 5 |
5 и более, но меньше 15 |
15 и более, о меньше 30 | 30 и более |
Данная классификация имеет простое и логичное клиническое обоснование. Полученные в результате ряда крупных эпидемиологических исследований, наиболее известным и масштабным из которых является Wisconsin Sleep Cohort Study (1988-2015), данные свидетельствуют, что именно с пяти аномальных респираторных эпизодов за час сна начинает постепенно проявляться характерная для СОАС клиническая симптоматика. В группе же пациентов с индексом апноэ-гипопноэ ≥15 постепенно начинает увеличиваться, а при индексе апноэ-гипопноэ ≥30 возрастает в разы вероятность возникновения сердечно-сосудистых осложнений, в том числе приводящих к смертельному исходу.
Это принципиально важно с практической точки зрения. Как показано в исследовании
J.M. Marin et al. (2005), наличие достоверно более высокого риска в отношении сердечно-сосудистой заболеваемости и смертности пока что можно считать однозначно доказанным только для пациентов с тяжелой формой СОАС, а коррекция у них нарушений дыхания во время сна возвращает эти риски к средним по популяции. Таким образом, первоочередной задачей амбулаторно практикующего врача становится выявление и лечение пациентов именно с тяжелым вариантом апноэ сна.
СОАС относится к числу широко распространенных патологических состояний и может встречаться в любом возрасте с детских лет до старости, но наиболее часто наблюдается в возрастной категории от 40 до 65 лет. Обобщая имеющиеся в литературе эпидемиологические данные Cao M. T. еt al. (2011) приходят к заключению, что в экономически развитых странах СОАС страдает порядка 8% населения. При этом вероятность возникновения обструктивного апноэ сна возрастает пропорционально возрасту и весу обследуемых. У пациентов без ожирения причиной СОАС могут стать врожденные особенность строения лицевого скелета – микро- и ретрогнатия или патология глотки – например значительная гипертрофия миндалин при хроническом тонзиллите. Кроме того, у мужчин среднего возраста СОАС возникает в 2-3 раза чаще, чем у женщин. У последних заболевание обычно развивается позднее, после менопаузы. Таким образом, наиболее типичный пациент с обструктивным апноэ сна – это мужчина среднего возраста с избыточным весом.
Еще несколько важных для практикующего терапевта моментов. В большой серии зарубежных исследований было показано наличие СОАС у 20-40% больных с артериальной гипертонией, хронической ишемической болезнью сердца, с инфарктом миокарда и инсультом в анамнезе, т.е. у значительной части контингента, обычного для клиники внутренних болезней. Кроме того, есть основания полагать, что две трети пациентов с СОАС не попадают в поле зрения врачей вплоть до возникновения у них тяжелых сердечно-сосудистых осложнений. Причем это данные по Западной Европе и Северной Америке, где медицина сна на сегодняшний день получила наибольшее развитие.
Результаты наших собственных исследований позволяют говорить о том, что до трети больных, обращающихся за помощью к отечественным врачам терапевтических специальностей, страдают СОАС, что опять же значительно выше, чем в общей популяции. При этом обращало на себя внимание, что ни у одного из пациентов, прошедших обследование в рамках этого научного проекта, СОАС ранее не только не был диагностирован, но даже предположен, несмотря на то, что во многих случаях это можно было легко сделать исходя из типичных клинических признаков. Хотя СОАС является опасной и широко распространенной патологией, это заболевание нашим врачам все еще недостаточно хорошо известно. В результате правильный диагноз ставится со значительным опозданием или не ставится вовсе, а пациенты не получают своевременного и адекватного лечения.
Одной из причин, предрасполагающих, на наш взгляд, к совершению подобных диагностических ошибок, является недопонимание частью отечественных клиницистов того, с каким же заболеванием они сталкиваются на практике. Вплоть до настоящего времени понятие СОАС во врачебном сознании часто ассоциируется с синдромом Пиквика. История этого вопроса такова. В середине прошлого века C. S. Burwell et al. (1956) описали больного с хронической дыхательной недостаточностью, легочным сердцем, дневной сонливостью и ожирением. По аналоги с вечно спящим толстяком Джо из романа Ч. Диккенса «Посмертные записки пиквикского клуба» данное клиническое состояние получило название пиквикского синдрома. Исследователи сочли, что причиной всех наблюдавшихся ими расстройств стала хроническая дыхательная недостаточность на фоне морбидного ожирения и именно такое понимание данного патологического состояния закреплено на сегодняшний день в Международной классификации болезней. И только спустя годы у пациентов с пиквикским синдромом были выявлены специфические нарушения дыхания во время сна, что позволило C. Guilleminault et al. (1973) сформулировать современную концепцию СОАС.
Так как обструктивные нарушения дыхания во время сна первоначально были описаны именно у больных с синдромом Пиквика и действительно встречаются у таких пациентов очень часто, многие специалисты стали ставить знак равенства между двумя этими понятиями. Более того, столь живо изображенный Ч. Диккенсом храпящий и сонливый слуга Джо, который послужил прототипом для авторов пиквикского синдрома, судя по описанию страдал именно СОАС, а не синдромом ожирения-гиповентиляции, т.е. с позиций современной классификации болезней, как ни парадоксально это прозвучит, «пиквиком» по всей видимости не являлся. Все это в течение многих лет регулярно становилось причиной терминологической путаницы.
СОАС и нарушения механики дыхания играют самостоятельную роль в происхождении респираторных нарушений, которые могут возникать у пациентов с ожирением. Исходя из современных представлений о нарушениях дыхания во время сна, следует четко понимать, что существуют СОАС, синдром ожирения-гиповентиляции или синдром Пиквика и их комбинация. Эти состояния во многом близки клинически, но нуждаются в дифференцированном подходе и различном лечении.
Связанные с обструктивным апноэ сна симптомы принципиально можно разделить на две группы – ночные и дневные (табл. 2).
Таблица 2. Основные симптомы СОАС [Cao M. T. еt al., 2011].
| НОЧНЫЕ СИМПТОМЫ | ДНЕВНЫЕ СИМПТОМЫ |
|
Храп Остановки дыхания Пробуждения, иногда с ощущением нехватки воздуха Гастроэзофагеальный рефлюкс и ассоциированные симптомы Учащенное мочеиспускание Повышенная двигательная активность Потливость Сухость во рту Гипнагогические галлюцинации |
Избыточная дневная сонливость Утренние головные боли Ощущение усталости и разбитости после пробуждения и в течение дня Ухудшение памяти, снижение способности к концентрации внимания, раздражительность, депрессия Снижение полового влечения и потенции |
Храпом называют звук, возникающий в результате вибрации мягких тканей верхних дыхательных путей при прохождении через них потока воздуха во время сна. Он является одним из наиболее характерных клинических маркеров сонного апноэ и согласно N. J. Douglas (1993) наблюдается у 95% больных с СОАС. Исключение могут составлять отдельные пациенты с морбидным ожирением, кифосколиозом и другими патологическими состояниями, приводящими к грубым нарушениям механики дыхания, в результате которых они оказываются не в состоянии генерировать усилие вдоха, достаточное для того, чтобы вызвать храп.
Принято различать неосложненный храп, при котором имеющий место звуковой феномен не сопровождается значимыми ограничениями воздушного дыхательного потока и храп, ассоциированный с нарушениями дыхания во время сна. Не все храпящие люди страдают СОАС, но практически все пациенты с обструктивным апноэ сна храпят. И если в первом случае, согласно классификации Американской академии медицины сна (2014), храп рассматривается как изолированный симптом в рамках нормы, то во втором он является признаком серьезного заболевания. Причем следует иметь ввиду, что апноэ сна может длительное время проявляться лишь громким храпом и только спустя годы трансформироваться в развернутый симптомокомплекс, типичный для пациента с СОАС. При этом бывает достаточно сложно уловить момент, когда храп с небольшим числом дыхательных пауз превращается в клинически значимый СОАС. В этой связи представляется интересной концепция Lugaresi E. et al. (1997) полагающих, что неосложненный храп и тяжелая форма обструктивного апноэ сна есть два крайних полюса одного, единого своей патофизиологической сущностью континуума, и поэтому следует объединить их под общим названием «болезнь громкого храпа». С практической точки зрения такой подход актуален для любого врача-интерниста тем, что дает понимание – храп часто бывает небезобиден и каждый храпящий больной должен автоматически вызывать настороженность в отношении потенциально возможных нарушений дыхания во время сна.
Остановки дыхания во время сна сравнительно редко оказываются среди первоочередных жалоб, с которыми страдающие СОАС пациенты обращается к врачу. Напротив, как было показано в работе V. Hoffstein et al. (1993), близкие родственники больных СОАС замечают у них остановки дыхания во время сна в 75% случаев. Иногда партнеры по спальне говорят не о дыхательных паузах, но описывают громкий храп, перемежается периодами тишины, которые также соответствуют эпизодам апноэ.
Беспокоящие некоторых пациентов с СОАС периодические ночные пробуждения от нехватки воздуха нередко трактуются врачами, в зависимости от возраста и анамнеза больного, как проявления кардиальной или бронхиальной астмы. Дифференциальная диагностики в этом случае достаточно проста даже без дополнительного обследования. В отличии от диспноэ сердечно-сосудистого или бронхолегочного генеза, связанное с предшествующим эпизодом апноэ ощущение нехватки воздуха не сопровождается затрудненным дыханием, хрипами в груди или положением ортопноэ и очень быстро проходит самостоятельно.
Повышение давления в брюшной полости во время сопровождающих обструктивные апноэ неэффективных дыхательных усилий нередко приводить к забросу в пищевод желудочного содержимого. Чаще всего такие больные жалуются на изжогу при пробуждениях. Описываемое при этом ощущение жжения за грудиной у пациентов старших возрастных групп иногда требует дифференциальной диагностики с ночной стенокардией. Неэффективность нитроглицерина и быстрое купирование симптомов после приема антацидных препаратов позволяют достаточно просто определиться с причиной беспокоящих пациента жалоб.
В более тяжелых случаях возможно попадание микрочастиц желудочного содержимого в верхние дыхательные пути, что клинически проявляется кашлем или ларингоспазмом. Периодические приступы кашля во время сна являются характерным симптомом гастроэзофагеального рефлюкса или бронхиальной астмы и сравнительно редко встречается при других заболеваниях. Отсутствие обратимой обструкции бронхов при исследовании функции внешнего дыхания и обычно выявляемые при гастроскопии признаки эзофагита помогают определиться с природой предъявляемых пациентом жалоб.
Ассоциированный с рефлюксом ларингоспазм является нечастым, но, наверное, наиболее драматичным состоянием среди симптомов, возникающих у больных с СОАС во время сна. Пациент рассказывает про внезапное пробуждение от удушья, резкое затруднение вдоха и выдоха, громкое стридорозное дыхание, чувство паники или даже страх смерти. Обычно приступ длится не более нескольких минут и проходит самостоятельно, но нередко столь сильно пугает больного, что ему бывает затруднительно объективно оценить истинную тяжесть и длительность произошедшего события. В большинстве случаев описываемая симптоматика ларингоспазма весьма специфична и диагноз не вызывает сомнений.
Клиническая картина, обусловленная рефлюксом, у пациентов с СОАС мало чем отличается от таковой при обычной гастроэзофагеальной рефлюксной болезни, но с одной поправкой – у пациентов с апноэ сна ночная симптоматика преобладает. Кроме того, специфика патогенетических механизмов в случае с СОАС предрасполагает к более упорному и рецидивирующему течению заболевания.
Никтурия является еще одним частым спутником СОАС. По мнению J. Krieger (1998), сопутствующие обструктивным апноэ неэффективные попытки вдоха вызывают колебания внутригрудного давления, а возникающий при этом присасывыющий эффект в свою очередь приводит к увеличению венозного возврата к сердцу – так называемой центральной псевдогиперволемии и растяжению правого предсердия. В результате повышается секреция предсердного натрийуретического фактора и увеличивается образование мочи.
Частое мочеиспускание в течение ночи у мужчин часто ошибочно трактуется как проявление хронического простатита или аденомы предстательной железы. При этом дифференциальный диагноз дизурии в этом случае достаточно прост и основывается на том, что для аденомы характерны частые позывы с затрудненным мочеиспусканием и отхождением малого количества мочи, тогда как при СОАС мочеиспускание обильное, свободное и безболезненное. Мы неоднократно сталкивались с ситуацией, когда пациенты, прежде длительно наблюдавшиеся и безуспешно лечившиеся у урологов, после нормализация дыхания во время сна полностью избавлялись от этой неприятной проблемы.
Пациенты с СОАС часто недоумевают, почему утром после пробуждения они чувствуют себя неотдохнувшими независимо от того, сколько времени им удалось провести перед этим в постели. При этом так как вызываемые дыхательными паузами активации головного мозга не означают полного поведенческого пробуждения, значительная часть больных с СОАС не имеет представления об истинном масштабе проблем, которые возникают у них в течение ночи. Поэтому многие пациенты с сонным апноэ искренне считают, что спят хорошо. Однако отдельные больные с СОАС, напротив, могут обратиться к врачу именно с жалобами инсомнического характера и описывать тревожный сон с частыми пробуждениями и кошмарными сновидениями.
Ошибка, которую нередко совершают проводящие консультативный прием врачи, основывается на неправильной трактовке жалоб части пациентов с СОАС на плохое качество сна. Случается, что упоминание о беспокойном прерывистом сне приводит к назначению гипнотиков, в то время как многие препараты со снотворным и седативным действием, еще больше понижая тонус мышц, потенциально способны усугублять дыхательную недостаточность и утяжелять СОАС. В первую очередь речь идет о широко применяемых в терапевтической практике транквилизаторах – производных бензодиазепина. Чтобы избежать подобных ошибок, необходимо помнить, что нарушения сна – обширная и гетерогенная группа расстройств, а необдуманное применение снотворных средств может оказаться бесполезным или даже вредным.
Еще одним следствием хронической нехватки сна у пациентов с СОАС может стать вкрапление в бодрствование некоторых характерных для него феноменов. Это проявляется так называемыми гипнагогическими галлюцинациями – галлюцинациями засыпания, когда при переходе от бодрствования ко сну пациент видит напоминающие сновидения образы, но при этом все еще воспринимает окружающий его реальный мир.
Закономерным результатом нарушения нормальной структуры сна у больных с СОАС становится избыточная дневная сонливость. Однако так как это ощущение является достаточно субъективным, часть пациентов с СОАС не вполне критично относится к своему состоянию и может преуменьшать степень имеющейся у них сонливости либо, напротив, даже гордится способностью спать в любом месте и в любое время. Кроме того, надо иметь в виду, что многие больные на момент обращения к врачу успевают частично адаптироваться к своему состоянию, описывая его как ощущение разбитости или утомленности в течение дня. При этом они могут не считать свою постоянную усталость чем-то необычным, стандартно находя ей объяснение в интенсивном ритме жизни и перегрузках на работе.
Однако сонливость становится очевидной, когда пациент находится в расслабленном состоянии, и проявляется засыпаниями во время послеобеденного отдыха, чтения или просмотра телепрограмм. При крайне выраженной сонливости возможны засыпания во время активной деятельности – беседы, еды, работы или вождении автомобиля. Из-за этого существенно повышается риск несчастных случаев. Результаты проведенного S. Tregear et al. (2009) мета-анализа свидетельствуют, что вероятность попасть в дорожно-транспортное происшествие у водителя с обструктивным апноэ сна возрастает в 4 раза.
Нарушения сна, дневная сонливость и воздействие гипоксии на головной мозг приводят к тому, что у больных СОАС часто наблюдаются интеллектуальные и эмоционально-личностные нарушения, такие как ухудшение памяти, расстройство внимания, неспособность к обучению, депрессия, тревога и раздражительность. Обструктивное апноэ сна может вызывать снижение полового влечения и нарушения потенции.
Сочетание галлюцинаций, кошмарных сновидений, эмоциональная лабильность, прогрессирующее снижение интеллекта в сочетании с периодическими приступообразными засыпаниями иной раз даже во время разговора с лечащим врачом обычно производят на малознакомого с этой патологией доктора сильное впечатление и могут ввести в заблуждение не только терапевта, но и психиатра. Нам довелось наблюдать пациентку, которая до этого в течение нескольких лет безуспешно лечилась у психоневролога. Выявление у нее тяжелой формы СОАС и последующее адекватное лечение в течение короткого времени привели к нормализации ее самочувствие и позволили вернуться к активной трудовой деятельности.
На сегодняшний день не вызывает сомнения факт патогенетической связи между обструктивным апноэ сна и повышением артериального давления. Более того, в отчете Объединенного национального комитета США по профилактике, диагностике, оценке и лечению повышенного артериального давления (2003) СОАС назван наиболее частой причиной вторичной артериальной гипертензии.
Ассоциация между артериальной гипертонией и СОАС стала предметом согласительного документа Европейского общества по артериальной гипертонии и Европейского респираторного общества (2012). В опубликованных ими совместных рекомендациях не только подтверждается наличие очевидной связи между гипертонией и обструктивным апноэ сна, но и признается, что СОАС ответственен за большую часть случаев повышения артериального давления или отсутствия его снижения в ночное время.
По данным E. C. Fletcher (1995) повышение артериального давления в бодрствовании наблюдается у половины больных с СОАС, и в этой группе встречается в два раза чаще, чем в популяции в целом. Отсутствие должной настороженности терапевтов и кардиологов в отношении нарушений дыхания во время сна приводит к тому, что у трети якобы страдающих эссенциальной гипертонией пациентов имеется недиагностированный СОАС.
Считается, что для пациентов с СОАС более характерна диастолическая артериальная гипертония с высокими цифрами артериального давления уже на момент пробуждения и его последующим снижением иногда даже без использования лекарственных средств, в результате чего утреннее артериальное давление может оказаться выше, чем в вечерние часы. Однако по нашим наблюдениям не менее частой находкой становится систолодиастолическая артериальная гипертония с высокими цифрами артериального давления как с утра, так и вечером.
При этом артериальная гипертония у пациентов с обструктивным апноэ сна нередко плохо поддается медикаментозному лечению. В работе H.K. Walia et al. (2014) показано, что при сочетании артериальной гипертонии с тяжелой формой апноэ сна вероятность резистентности к гипотензивным препаратам повышается в 4 раза. Российские рекомендации по диагностике и лечению артериальной гипертензии (2010) также указывают, что у всех пациентов с неподдающейся лечению артериальной гипертонией надо учитывать вероятность наличия СОАС. Наш опыт показывает, что даже в тех случаях, когда медикаментозная терапия позволяет нормализовать цифры артериального давления в течение дня, у части пациентов с СОАС к утру оно вновь оказывается повышенным и только нормализация дыхания во время сна дает возможность адекватно контролировать у них величину артериального давления в течение всех суток.
Однако так как оба патологических состояния широко распространены в популяции, то возможно их случайное сочетание и наличие артериальной гипертонии у пациента с СОАС не позволяет автоматически говорить о причинно-следственной связи между повышением артериального давления и дыхательными нарушениями во время сна. В этой связи нам представляется целесообразным говорить про апноэ-зависимую и апноэ-независимую гипертонию. Первая группа преимущественно включает пациентов с ночной и утренней артериальной гипертонией, которая часто нечувствительна к лекарственной терапии, но в значительной мере облегчается после устранения СОАС. Обычно это сравнительно более молодые больные с тяжелой формой апноэ сна. Во второй группе больные обычно старше и демонстрируют свойственное эссенциальной гипертонии преимущественное повышение артериального давления во второй половине дня. Коррекция СОАС у них не приводит к существенному снижению артериального давления, но у них наблюдается адекватный ответ на медикаментозную терапию. Если у пациентов первой группы лечение артериальной гипертонии невозможно без нормализации дыхания во время сна, то представители второй требуют подбора медикаментозной терапии вне зависимости от лечения СОАС.
Частая встречаемость обструктивных нарушений дыхания во время сна при отсутствии на сегодняшний день реальной возможности провести специальное углубленное обследование всем потенциально нуждающихся в этом больным обуславливает необходимость выработки оптимальных принципов выявления апноэ сна сотрудниками медицинских учреждений терапевтического профиля, в том числе и в амбулаторной практике. При этом, исходя из имеющихся на сегодняшний день доказательств роли тяжелой формы СОАС в формировании опасных сердечно-сосудистых осложнений, можно сказать, что внимание и усилия врачей терапевтических специальностей должны быть сосредоточены на первоочередном выявление именно этой категории больных.
Применительно к амбулаторной практике, наиболее рациональной нам представляется концепция ступенчатого подхода к диагностике СОАС, согласно которой в начале определяются пациенты с высоким риском апноэ сна, затем среди них проводится скрининговое исследование для выявления больных с вероятным СОАС, и в конце у отобранных пациентов диагноз подтверждается или исключается с помощью специальных методов обследования.
Предлагаемый нами алгоритм поэтапного диагностического поиска иллюстрирует, каким образом это можно сделать, исходя из реальных возможностей, которыми в настоящее время располагают отечественные врачи-терапевты (алгоритм 1).
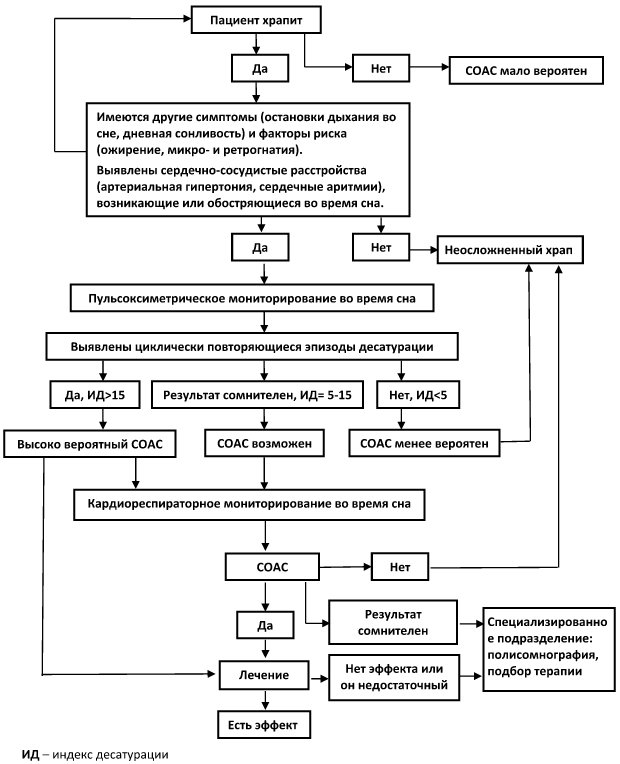
Алгоритм 1. Поэтапный диагностический поиск для выявления СОАС в амбулаторной практике врача-терапевта
Сочетание храпа, остановок дыхания во время сна и избыточной дневной сонливости в той или иной комбинации наблюдается практически у всех больных с СОАС, составляет клиническое ядро данного синдрома и является отправной точкой диагностического поиска. Однако, получить достоверную информацию о наличии этих симптомов не столь просто, как это может показаться с первого взгляда.
Говоря о наличии или отсутствии храпа, пациент вынужден обсуждать с врачом события, происходящие с ним во время сна и известные ему преимущественно со слов окружающих. Опыт показывает, что если одновременно опрашивать и родственников больного, то в итоге количество храпящих увеличивается как минимум в полтора раза. Хотя понятно, что вероятность последующего обнаружения клинически значимых нарушений дыхания во время сна у пациентов с регулярным громким храпом будет существенно выше, имеет смысл принимать во внимание сообщения о храпе любой периодичности и интенсивности. Более того, как уже обсуждалось ранее, даже отсутствие храпа не всегда позволяет полностью исключить у пациента СОАС, хотя и делает этот диагноз существенно менее вероятным.
Остановки дыхания во сне сравнительно редко оказываются среди тех жалоб, которые пациент с СОАС активно предъявляет своему врачу. Однако при целенаправленном расспросе выясняется, что периоды апноэ во время сна окружающие замечают более чем у трети из них. Впрочем, этот признак может быть не свидетельством патологии, а лишь отражать дыхательную аритмию, которая в норме наблюдается во время стадии быстрого сна.
Вопрос об избыточной дневной сонливости следует формулировать максимально четко и развернуто. Дело в том, что длительно болеющие люди привыкают к своему состоянию, искренне считают, что у них нет никакой сонливости, и дадут отрицательный ответ на прямой вопрос о ее наличии. Поэтому следует говорить с больным о желании уснуть применительно к разным повседневным ситуациям. Именно по такому принципу построена так называемая Эпвортская шкала дневной сонливости. Предложенная M. W. Johns (1991) анкета получила широкое распространение как простой и достаточно точный инструмент количественной оценки этого симптома. Опросник предлагается пациенту оценить возможность задремать или даже уснуть в различных жизненных ситуациях и оценить вероятность этого в баллах (0 – никогда; 1 – небольшая вероятность; 2 – умеренная вероятность; 3 – высокая вероятность):
- Чтение сидя
- Просмотр телепередач
- Пассивное участие в общественных мероприятиях (в театре, на собрании и т.д.)
- Как пассажир в машине (если поездка длится не менее часа)
- Если прилечь отдохнуть после обеда в отсутствии других дел
- Сидя или разговаривая с кем-либо
- Сидя спокойно после еды (без употребления спиртного)
- За рулем автомобиля, остановившегося на несколько минут в дорожной пробке
Затем все баллы суммируются. Получившаяся в итоге величина характеризует степень дневной сонливости, которая у пациентов с СОАС в среднем составляет 12 баллов. Однако, согласно данным И.М. Воронина (2001), уже при сонливости более 5 баллов индекс апноэ-гипопноэ часто оказывается выше нормы, а сонливость более 10 баллов расценивается как значительная и на практике обычно соответствует выраженному СОАС.
Однако, даже при таком подходе некоторые пациенты могут не вполне адекватно оценивать свою сонливость, преуменьшая ее. Кроме того, хотя полученная при расчете с помощью Эпвортской шкалы величина в целом коррелирует с индексом апноэ-гипопноэ, степень сонливости может значительно варьировать у больных с одинаковой тяжестью дыхательных нарушений во время сна, что не позволяет однозначно установить наличие и определить истинную тяжесть СОАС. И, конечно же, следует помнить, что избыточная дневная сонливость не является симптомом, патогмоничным для обструктивного апноэ сна, и может встречаться при других, преимущественно неврологических, заболеваниях.
Основой последующего правильного диагноза обструктивного апноэ сна являются верно заданные врачом вопросы. Упростить процесс сбора специфических жалоб и анамнеза можно используя специальные опросники. Существуют анкеты, специально адаптированные для первичного выявления пациентов с риском СОАС. Они удобны тем, что помогают не упустить характерные для обструктивного апноэ сна симптомы вне зависимости от субъективных представлений человека о своем заболевании и степени специальной подготовки врача. Так, например, при наличии трех или более специфических симптомов и признаков, таких как:
- Указания на остановки дыхания во сне
- Громкий храп
- Периодические пробуждения с чувством нехватки воздуха
- Учащенное мочеиспускание ночью
- Тревожный неосвежающий сон
- Чувство разбитости или головные боли по утрам
- Дневная сонливость
- Снижение работоспособности, памяти и внимании
- Наличие артериальной гипертонии
- Избыточный вес – индекс массы тела более 30 кг/м2 и окружность шеи более 43 см.
- Возраст старше 40 лет для мужчин и старше 50 лет для женщин
пациент, вероятно, страдает обструктивным апноэ сна и ему необходимо пройти специальное обследование.
При этом следует помнить, что одних только клинических признаков в большинстве случаев недостаточно для того, чтобы однозначно диагностировать СОАС и, главное, точно определить его тяжесть. Хотя в типичных, наиболее тяжелых случаях диагноз представляется вполне очевидным уже на основании клинической картины заболевания, достоверно отличить всех пациентов с СОАС с помощью какого-либо даже самого подробного опросника не представляется возможным. Не существует симптоматики, абсолютно специфичной для обструктивного апноэ сна. Кроме того, практически не встречаются пациенты у которых одновременно присутствовали бы абсолютно все характерные для СОАС признаки, а наблюдающиеся комбинации симптомов разнообразны и непредсказуемы. Правильный сбор жалоб и анамнеза заболевания лишь помогают отобрать лиц с повышенным риском обструктивного апноэ сна для дальнейшего, более детального их обследования.
На этапе первичного выявления пациентов из группы риска нужно как можно более полно использовать возможности рутинных в терапевтической практике инструментальных методов обследования.
Определенную полезную для последующей диагностики апноэ сна информацию можно получить, анализируя результаты суточного мониторирования артериального давления. Достаточно характерным для СОАС признаком является отсутствие физиологического снижения давления во время сна по сравнению с периодом бодрствования. Причем значительное ночное повышения артериального давления косвенно говорит о тяжести имеющих место дыхательных расстройств. Так как СОАС является одной из наиболее частых причин, приводящих к подобным изменениям суточного профиля артериального давления, таким больным показано дальнейшее более углубленное обследование, особенно если имеется соответствующая симптоматика или дополнительные факторы риска. Однако следует понимать, что наличие ночной гипертонии повышает вероятность последующего обнаружения СОАС, но ее отсутствие не позволяет исключить дыхательные нарушения во время сна у обследуемого больного.
Весьма информативными могут оказаться результаты холтеровского мониторирования ЭКГ. В работе C. Guilleminault et al. (1983) и ряде последующих исследований было показано, что для пациентов с СОАС характерны различные нарушения ритма и проводимости сердца во время сна – частая экстрасистолия, суправентрикулярные тахиаритмии, синусовые паузы, эпизоды неустойчивой желудочковой тахикардии и атриовентрикулярная блокада II степени. При этом по данным R. Mehra et al. (2006) вероятность ночных аритмий у пациентов с сонным апноэ в 2-4 раза выше по сравнению с контролем. Таким образом, возникающие преимущественно во время сна нарушения проводимости и ритма сердца справедливо считаются одним из значимых клинических маркеров СОАС.
У большой части пациентов с СОАС эпизоды апноэ сопровождает синусовая аритмия, характеризующаяся прогрессирующей брадикардией, в отдельных наиболее тяжелых случаях вплоть до асистолии, которая резко сменяется тахикардией после возобновления легочной вентиляции. Эта аритмия не является отражением какого-либо заболевания сердца. Согласно C. Zwillich et al. (1982), причиной ассоциированной с эпизодами обструктивного апноэ бради-тахикардии является так называемый «рефлекс ныряльщика», в соответствии с которым гипоксия вызывает брадикардию или тахикардию в зависимости от отсутствия или наличия легочной вентиляции. Кроме того, сопровождающее возобновление дыхания повышение симпатического тонуса вносит дополнительный вклад в генез возникающей после окончания апноэ компенсаторной тахикардии.
Провоцируемую апноэ сна брадикардию и синусовые паузы (рис. 1) иногда неверно трактуют как проявление синдрома слабости синусового узла. Избежать подобной ошибки поможет тот факт, что связанная с обструктивным апноэ брадиаритмия возникает только во время сна, в то время как в бодрствовании в большинстве своем страдающие ожирением пациенты с СОАС склонны к тахикардии, что абсолютно не укладывается в концепцию дисфункции синусового узла. Тем не менее, нередки случаи, когда неправильная трактовка причины подобных нарушений приводит к необоснованной имплантации искусственного водителя ритма. Так в исследовании S. Garrigue et al. (2007) было установлено, что у 59% пациентов с установленным ранее кардиостимулятором имеется СОАС. Обсуждая полученные результаты, авторы делают заключение, что даже если не у всех этих больных брадиаритмии были напрямую связаны с апноэ сна, у потенциальных кандидатов на установку искусственного водителя ритма следует по умолчанию исключать СОАС.
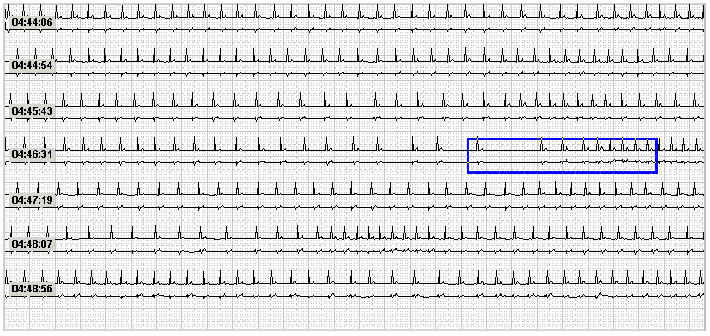
Рисунок 1. Холтеровское мониторирование у пациента с тяжелым СОАС – связанная с эпизодами обструктивного апноэ синусовая аритмия во время сна
Регистрируемые у пациентов с СОАС циклически повторяющиеся колебания частоты сердечных сокращений во время сна столь характерны, что некоторые производители оборудования для холтеровского мониторирования включают в поставляемое программное обеспечение особую опцию, предназначенную для того, чтобы выявлять апноэ сна. Наш опыт показывает, что данные программные продукты пока далеки от совершенства, их возможности не выходят за рамки простейшего скрининга и их не следует рассматривать в качестве независимого и объективного метода диагностики нарушений дыхания во время сна.
На сегодняшний день существует ряд существенно отличающихся друг от друга по своим техническим характеристикам диагностических устройств, позволяющих объективно измерять различные параметры дыхания во время сна и с той или иной точностью выявлять имеющиеся респираторные нарушения. Согласно рекомендациям Американской академии медицины сна (2009) это оборудование принято подразделять на 4 типа (табл.3).
Таблица 3. Медицинское оборудование, которое потенциально может быть использовано для диагностики СОАС [L. J. Epstein et al., 2009].
| Тип | Наименование | Характеристика | Регистрируемые показатели |
| Тип 1 | Стационарная полисомнография. | Проводится в условиях специализированного медицинского подразделения под постоянным контролем медицинского персонала. | Объективизация сна, параметры дыхания и сердечной деятельности, двигательная активность |
| Тип 2 | Портативная полисомнография. | Может проводиться как амбулаторно, так и в условиях стационара любого профиля. | Объективизация сна, параметры дыхания и сердечной деятельности, двигательная активность |
| Тип 3 | Кардиореспираторное мониторирование. | Может использоваться как для амбулаторных исследований, так и в условиях стационара любого профиля. | Параметры дыхания и сердечной деятельности |
| Тип 4 | Одно- или двухканальные мониторы. | Чаще служат для амбулаторных исследований, но иногда могут применяться в условиях стационара. | Воздушный поток и SaO2 или только пульсоксиметрия |
Полисомнография является общепризнанным «золотым стандартом» в диагностике различных расстройств, связанных со сном. Исследование представляет собой синхронную регистрирацию во время сна электроэнцефалограммы, электроокулограммы, подбородочной электромиограммы, воздушного потока на уровне рта и носа, дыхательных движений живота и грудной клетки, сатурации кислорода, электрокардиограммы и двигательной активности ног. Первые три из вышеперечисленных показателей являются базовыми для идентификации фаз и стадий сна. Существуют портативные модели полисомнографов, рассчитанные на использование не только в стационаре, но и в амбулаторных условиях. Результаты исследования дают очень точную картину различных нарушений, возникающих во время сна, и в том числе позволяют выявить наличие, характер и длительность аномальных респираторных эпизодов, сопровождающие их нарушения сердечного ритма и снижение насыщения крови кислородом, а также соотношение всех этих феноменов с фазами сна.
Однако применение полисомнографии не сегодняшний день ограничено высокой стоимостью аппаратуры и нехваткой специалистов, имеющих соответствующую подготовку в этой области. В результате количество медицинских учреждений, имеющих возможность проводить такие исследования, в сравнении с существующими потребностями несоизмеримо мало. Причем эта проблема не является исключительно российской. Так, например, в рекомендациях Канадского торакального общества (2011) прямо указывается, что среднее время ожидания пациентом в очереди на полисомнографию составляет в этой стране около года, причем есть отдельные регионы, где проведение адекватного сомнологического обследования до настоящего времени вообще невозможно. Авторы руководства делают заключение, что в отношении пациентов с СОАС выходом из этой ситуации может стать использование альтернативных, более простых и доступных диагностических стратегий.
Применительно к имеющимся в арсенале отечественного врача-интерниста методам инструментального исследования для скрининга пациентов с СОАС может быть использована пульсоксиметрия во время сна. Такие устройства компактны, просты в применении и легко могут быть использованы для проведения амбулаторных обследований.
Пульсоксиметрическое мониторирование позволяет зарегистрировать сопровождающие апноэ и гипопноэ циклически повторяющиеся эпизоды гипоксемии (рис. 2). Для описание результатов исследования используется индекс десатурации, рассчитываемый как среднее число падений сатурации кислорода на 4% и более от исходной за час сна. При этом нередко ставится условный знак равенства между индексом десатурации и индексом апноэ-гипопноэ, что не всегда правомочно. Дело в том, что выраженность ассоциированной с апноэ гипоксемии многофакторна и ее степень может значительно варьировать у разных больных, так что респираторные паузы не всегда сопровождаются значимой десатурацией и в этом случае не могут быть выявлены с помощью пульсоксиметрии.
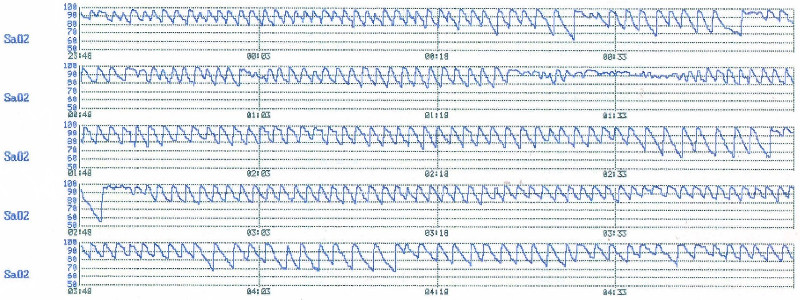
Рисунок 2. Пульсоксиметрическое мониторирование во время сна у пациента с тяжелым СОАС. Видны циклически повторяющиеся эпизоды десатурации.
Отношение к пульсоксиметрии, как самостоятельному методу объективизации дыхательных нарушений во время сна на сегодняшней день крайне противоречиво не только среди отдельных специалистов, но и на уровне национальных рекомендаций. Не прекращается дискуссия о целесообразности пульсоксиметрического мониторирования для первичной диагностики СОАС. Высказываемые мнения варьируют от полного отрицания этого метода до возможности использовать результаты ночной пульсоксиметрии для постановки окончательного диагноза СОАС. Так, например, согласно рекомендациям Американской академии медицины сна (2003), пульсоксиметорическое мониторирование не следует применять для диагностики СОАС из-за недостаточной чувствительности и специфичности этой методики, в то время как эксперты Канадского торакального общества (2011) считают возможным использовать результаты пульсоксиметрии не только для скрининга, но даже для постановки окончательного диагноза обструктивного апноэ сна у отдельных пациентов с типичной клинической симптоматикой.
Проанализировав ряд работ, посвященных диагностической роли пульсоксиметрии у пациентов с СОАС, мы пришли к выводу, что в основе столь противоречивых выводов лежат различия целей, дизайна и методологии проведенных исследований. Во-первых, большую роль играет дискретность регистрации сигнала – в идеале она должна составлять 1-2 секунды. В противном случае информативность и достоверность результатов обследования ощутимо падает. Во-вторых, чувствительность и специфичность пульсоксиметрического мониторинга в значительной степени зависит от характеристик обследуемой клинической популяции. Если у пациентов с тяжелым СОАС получаемые результаты в подавляющем большинстве случаев практически идентичны таковым, как если бы для исследования использовалась многоканальная диагностическая система, то у больных с апноэ сна средней тяжести точность такого исследования будет ниже, а при легкой степени заболевания пульсоксиметрия вообще мало информативна. Таким образом, допущение, что индекс десатурации в полной мере описывает степень возникающих у обследуемого пациента дыхательных нарушений во время сна, применим только к больным с наиболее тяжелым течением СОАС. Соответственного, если авторы исследования задавались вопросом, позволяет ли пульсоксиметрия выявлять всех пациентов с апноэ сна, то ответ, естественно, получался отрицательным. Если же исследователи оценивали диагностические возможности пульсоксиметрического мониторирования по выявлению пациентов с клинически значимым СОАС, в этом случае ответ звучал положительно.
Важным практическим моментом является то, какое пороговое значения индекса десатурации следует рассматривать в качестве патологического. Мнение большинства изучавших этот вопрос специалистов совпадает с рекомендациями Британского торакального общества (1991), предлагающими считать индекс десатурация более 15 значимым предиктором СОАС.
Анализируя данные литературы Р. В. Бузунов и соавт. (2013) приходят к выводу, что пульсоксиметрический мониторинг может применяться для первичного выявления СОАС. Авторы подчеркивают – они понимают, что часть пациентов будет при этом пропущена, но это все равно станет огромным шагом вперед по сравнению с текущей ситуацией, когда апноэ сна в отечественном практическом здравоохранении за редкими исключениями не диагностируется вовсе.
Таким образом, можно заключить, что применительно к амбулаторной практике пульсоксиметрическое мониторирование во время сна можно рассматривать в качестве пусть не самого точного, зато простого, доступного и, что немаловажно, наиболее дешевого метода для первичной диагностики СОАС. Следует еще раз подчеркнуть, что первоочередной целью терапевта на сегодняшний день является выявление пациентов с наиболее тяжелыми, чреватыми жизнеугрожающими осложнениями формами апноэ сна и применительно к этой задаче результаты пульсоксиметрии будут достаточно информативны.
Вопрос о том, можно ли иногда начинать специфическую терапию СОАС на основании диагноза, установленного только по результатам пульсоксиметрии, мы оставляем открытым. Действительно, большинство существующих на сегодняшний день практических руководств в лучшем случае отводят пульсоксиметрическому мониторированию вспомогательную роль, справедливо полагая, что наличие СОАС должно быть подтверждено с помощью специального более детализированного исследования. И мы полностью разделяем такую позицию в ситуации, когда речь идет о специализированном сомнологическом подразделении. Однако характерные результаты пульсоксиметрии во время сна в сочетании с типичной клинической симптоматикой у отдельных пациентов позволяют определиться с высоко вероятным диагнозом. И это будут наиболее тяжело больные люди, особенно нуждающиеся в медицинской помощи. При существующем в настоящее время дефиците медицинских центров соответствующего профиля, рекомендовать таким пациентам дополнительное обследование у сомнолога означает оставить часть из них без лечения. Врачу необходимо оценить доступность для больного специализированной медицинской помощи и только после этого принимать взвешенное решение.
Обнаруженные эпизоды гипоксемии во время сна указывают на наличие проблемы, но часто не позволяет однозначно определиться с ее первопричиной. Поэтому для окончательной верификации диагноза требуется более информативное исследование. На сегодняшний день для диагностики дыхательных расстройств во время сна в амбулаторных условиях наиболее оправданным представляется использование портативных кардиореспираторных мониторирующих систем, специально разработанных для диагностики нарушений дыхания во время сна. Минимальный набор параметров, которые регистрируются такими устройствами, включает храп, воздушный поток, дыхательные усилия, сатурацию кислорода и частоту сердечных сокращений, что в большинстве случаев позволяет поставить правильный диагноз (рис. 3). Техническая простота использования такого диагностического прибора позволяет после короткого инструктажа дать его пациенту на дом, перед сном тот самостоятельно закрепляет на теле необходимые датчики, а утром возвращает устройство врачу для анализа результатов исследования.
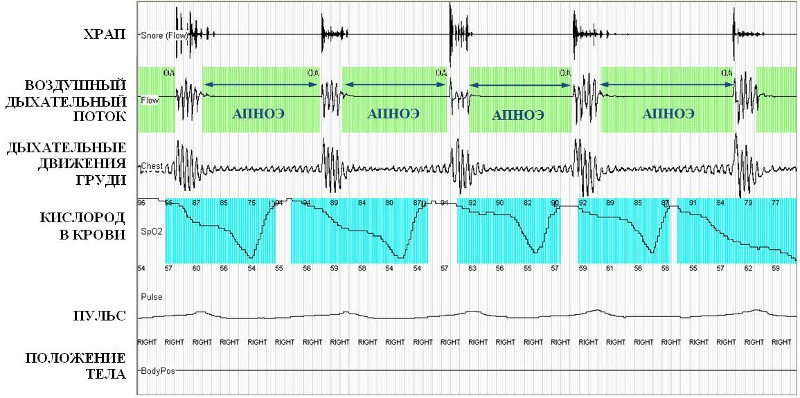
Рисунок 3. Результаты кардиореспираторного мониторировния при тяжелом апноэ сна (фрагмент записи). Исчезновение дыхательного потока происходит на фоне сохраняющихся дыхательных усилий, что подтверждает обструктивный характер регистрируемых респираторных эпизодов. Восстановление дыхания сопровождается интенсивным храпом.
Кардиореспираторное мониторирование во время сна, в том числе и проводимое амбулаторно, является общепризнанной и широко распространенной в мире диагностической методикой, простой в использовании, более дешевой по сравнению с полисомнографией и при этом достаточно информативной. Согласно принятым на сегодняшний день международным рекомендациям, это исследование, в первую очередь, показано пациентам с подозрением на клинически значимый СОАС, т.е. в тех случаях, когда, исходя из имеющейся симптоматики, можно сказать, что вероятность последующего выявления дыхательных нарушений во сне достаточно велика. Но это как раз и есть те самые больные, которые должны являться предметом первоочередного интереса специалистов терапевтических направлений.
Анализируя результаты кардиореспираторного мониторирования следует иметь ввиду, что подразделение респираторных событий на обструктивные и центральные только на основании характера дыхательных движений не всегда оказывается точным с клинической точки зрения. Видимое отсутствие дыхательных усилий не обязательно означает центральную природу имеющихся нарушений, так как для регистрации слабых дыхательных попыток иногда не хватает чувствительности датчиков, что нередко встречается у пациентов с тяжелым ожирением. В ситуации, когда эпизоды апноэ и гипопноэ сочетаются с интенсивным храпом, возникают преимущественно в положении на спине или у больных с выраженным ожирением, всегда существует вероятность, что в их основе лежит обструкция верхних дыхательных путей.
Иногда технических возможностей кардиореспираторного мониторирования может оказаться недостаточно. В частности, следует помнить, что эта методика не позволяет выявлять эпизоды гипопноэ, не сопровождающиеся значительным ограничением легочной вентиляции и выраженной десатурацией (так называемая повышенная сопротивляемость верхних дыхательных путей), так как для этого необходима энцефалографическая регистрация мозговых активаций. Кроме того, не всегда удается точно соотнести выявленные респираторные феномены с реальной длительностью сна, что у пациентов с жалобами инсомнического характера может привести к последующим диагностическим ошибкам. Поэтому в спорных случаях больной должен быть направлен в специализированное лечебное учреждение для проведения полисомнографии.
Завершая разговор об амбулаторной диагностике СОАС, хочется отметить, что ретроспективный анализ наиболее распространенных диагностических ошибок, совершаемых врачами терапевтических специальностей при столкновении со страдающими апноэ сна пациентами, позволяет нам сделать вывод, что встречающиеся неверные суждения чаще всего основываются на формальном подходе к оценке характерной для СОАС симптоматики. Наиболее частой причиной неадекватной диагностики обструктивного апноэ сна на сегодняшний день являются не столько объективные трудности диагностического поиска или нехватка соответствующего современного оборудования, сколько недостаточная настороженность врачей в отношении этой серьезной патологии. Знание факторов риска и клинической симптоматики СОАС – вот та основа, которая позволяет адекватно выявлять больных с апноэ сна, обращающихся за помощью в лечебные учреждения терапевтического профиля.
В последние годы международное медицинское сообщество выработало единые представления о показаниях к началу специфической терапии СОАС. Суммируя актуальные рекомендации профессиональных врачебных ассоциаций разных стран, можно сказать, что обязательным является лечение пациентов с тяжелым СОАС, желательным с апноэ сна средней тяжести и возможным при легкой форме сонного апноэ, особенно если у такого больного имеется характерная для апноэ сна клиническая симптоматики или ассоциированная сердечно-сосудистая патология. Рекомендации по выбору оптимального метода лечения также в большой степени основываются на исходной тяжести СОАС (алгоритм 2).
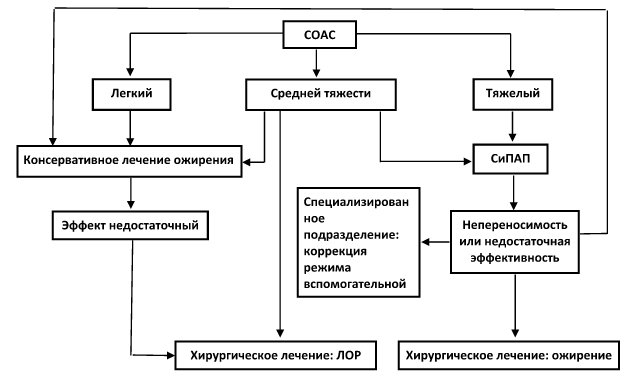
Алгоритм 2. Дифференцированный подбор терапии больным с СОАС
Коррекция ожирения является базовым принципом лечения любого пациента с СОАС и избыточной массой тела вне зависимости от тяжести заболевания. При этом следует стремиться к тому, чтобы вес снизился как минимум на 10% от исходного, а достигнутый в итоге индекс массы тела составлял 25 кг/м2 и менее. В этом случае можно ожидать значительное уменьшение индекса апноэ-гипопноэ вплоть до полной нормализации дыхания во время сна у некоторых пациентов.
Однако проблема заключается в том, что одних только диетологических мероприятий пациенту с выраженным ожирением и тяжелым СОАС часто бывает недостаточно. Этому имеется несколько объяснений. Во-первых, свойственные пациентам с апноэ сна сонливость и депрессия в сочетании с объективным снижением толерантности к физическим нагрузкам при ожирении резко ограничивают повседневную физическую активность и, соответственно, энергозатраты таких больных. Во-вторых, значительное число пациентов с выраженным ожирением имеет те или иные нарушения пищевого поведения и, в том числе, отсутствие самокритики к факту переедания, что может свести на нет любые диетические программы. И наконец, в-третьих, СОАС ведет к инсулинорезистентности и нарушению толерантности к глюкозе, так что многие пациенты с тяжелым апноэ сна часто оказываются физически не способны похудеть, пока у них не будут устранены имеющиеся нарушения дыхания.
Несколько особняком стоят хирургические техники, направленные на коррекцию ожирения. Бариатрическая хирургия потенциально показана и позволяет добиться значительного похудания у пациентов с жизнеугрожающим ожирением, когда предпринятые до этого консервативные попытки по снижению веса оказались неудачными. Следствием радикальной потери веса может стать одновременное исчезновение сонного апноэ. Однако хирургическое лечение ожирения не гарантирует полного избавления от СОАС. По данным J.I. Mechanick et al. (2008) через два года после проведенной бариатрической операции только у 40% пациентов наблюдается полная ремиссия СОАС.
Наш собственный взгляд на хирургические операции для коррекции ожирения применительно к пациентами с СОАС сводится к следующему. Как выраженное ожирение, так и апноэ сна обуславливают самостоятельные риски при любой хирургической операции. Соответственно при их сочетании вероятность осложнений оперативного вмешательстве еще больше увеличивается. При том, что на сегодняшний день существует гарантированно эффективный и безопасный способ нехирургического лечения СОАС, рассматривать бариатрическую хирургию в качестве самостоятельного и равноправного метода, направленного на лечение именно обструктивного апноэ сна нам представляется не вполне правильным. Более того, в ряде исследований было показано, что предварительная коррекция нарушений дыхания во время сна, возникающих на фоне морбидного ожирения, достоверно уменьшает риски последующих оперативных вмешательств. Хирургическое снижение веса можно рекомендовать отдельным пациентам с СОАС и тяжелой степенью ожирением в качестве альтернативного метода лечения в том случае, когда использование других, общепризнанных методик, оказалось по каким-либо причинам неприемлемо.
Несмотря на то, что идея медикаментозной коррекции СОАС изначально выглядела привлекательно со всех точек зрения, неоднократно предпринимавшиеся в этом направлении усилия врачей и фармакологов не увенчались успехом и эффективное лекарство найдено не было. Обсуждая со страдающим СОАС пациентом предстоящую стратегию лечения, следует сразу же донести до него мысль о бесполезности любых лекарственных препаратов, якобы позволяющих лечить храп, реклама которых периодически продолжает появляться в средствах массовой информации. На сегодняшний день существует три признанных врачебным сообществом, доказавших свою эффективность и получивших наибольшее распространение способов лечения сонного апноэ. Это хирургическое вмешательство на верхних дыхательных путях, использование внутриротовых аппликаторов и неинвазивная вспомогательная вентиляция во время сна. Все эти методы концептуально схожи тем, чтобы направлены на поддержание в раскрытом состоянии верхних дыхательных путей во время сна.
Хирургические пособия, позволяющие улучшать проходимость верхних дыхательных путей во время сна, исторически стали первой лечебной тактикой, реально позволявшей облегчить течение СОАС или даже полностью устранить нарушения дыхания во время сна. Первоначально W. Kuhlo et al. (1969) и E. Lugaresi et al. (1970) предложили лечить СОАС посредством трахеостомии, обеспечивая тем самым поступление воздуха в легкие минуя уровень возникающей обструкции глотки. Длительное время это был единственный по-настоящему эффективный метод лечения тяжелых форм СОАС. В дальнейшем S. Fujita et al. (1981) разработали операцию по коррекции анатомических аномалий глотки у больных с СОАС, названную увулопалатофарингопластикой. Она представлялась более щадящей альтернативой трахеостомии у больных с обструктивным апноэ сна и была направлена на увеличение воздушного пространства и проходимости глотки. Операция включает в себя удаление миндалин, сшивание нёбных дужек и иссечение нёбного язычка с частью мягкого нёба. Опубликованные авторами первые, весьма обнадеживающие данные о высокой эффективности такого лечения послужили толчком к широкому применению как самой увулопалатофарингопластики, так и других, близких по своей сути, но менее травматичных хирургических методик, в основе которых лежало лазерное, радиоволновое, холодовое или химическое воздействие на мягкотканные структуры ротоглотки. Однако достаточно быстро выяснилось, что увулопалатофарингопластика и ее вариации неэффективны у пациентов с выраженным ожирением и тяжелым СОАС, могут сопровождаться серьезными осложнениями, а достигнутое в ходе операции улучшение не всегда оказывается стойким.
Тем не менее, хирургические методы в настоящее время занимают прочное место в арсенале имеющихся способов борьбы с СОАС. При этом во всех современных клинических рекомендациях подчеркивается, что хирургические вмешательства на верхних дыхательных путях эффективны только в случае правильного отбора пациентов. Любой такой операции должно предшествовать тщательное обследование больного. Только после того, как будут выявлены анатомические аномалии верхних дыхательных путей и уточнена тяжесть СОАС, принимается индивидуализированное решение о возможности и объеме хирургического вмешательства. Потенциально такие операции могут быть предложены пациентам с легкой или среднетяжелой формой апноэ сна и не показаны при тяжелом СОАС.
Отдельно следует остановиться на проблеме неадекватного хирургического лечения сонного апноэ. Существует немало лечебных учреждений, обещающих практически любому обратившемуся к ним пациенту избавление от храпа после небольшой, в большинстве случаев проводимой амбулаторно, операции. На самом деле помогают они существенно реже, чем обещает реклама. Более того, возможна ситуация, когда в итоге такого неадекватного лечения храп действительно уменьшается, создавая у больного ложное ощущение благополучия, в то время как дыхательные нарушения во время сна остаются в прежнем объеме.
Причем похоже, что данная проблема носит интернациональный характер. Так в одном из своих руководств, посвященных хирургическому лечению СОАС, экспертами Американской академии медицины сна (2001) особый акцент делается на том, что лазерную увулопалатопластику следует исключить из перечня хирургических пособий, рекомендуемых для лечения обструктивного апноэ сна. В равной степени это следует отнести к любым другим малоинвазивным вмешательствам на мягком небе.
Обсуждая с пациентом возможный выбор хирургического метода лечения, следует подчеркнуть, что ни один грамотный и добросовестный хирург не станет давать однозначных гарантий, назначит специальное предварительное обследование, включающее диагностику потенциально возможных нарушений дыхания во время сна, если это не было сделано ранее, и будет говорить лишь о вероятности успеха.
Еще одним методом лечения апноэ сна являются внутриротовые аппликаторы – специальные механические устройства, предотвращающие коллапс глотки во время сна за счет выдвижения вперед нижней челюсти и удержания языка. Методика рассчитана на пациентов с легкой и среднетяжелой формой СОАС. В нашей стране данное терапевтическое направление непопулярно и малодоступно, так что в подробном его обзоре мы не видим практического смысла. Хотелось бы лишь упомянуть о том, что в продаже можно встретить уже готовые к использованию модели внутриротовых аппликаторов. Мы не рекомендуем своим пациентам приобретать подобные изделия. Единственно правильным является индивидуальный подбор и изготовление такого приспособления под конкретного больного квалифицированным стоматологом. В противном случае эффективность лечения за редкими исключениями будет низкая.
В 1981 году C. E. Sullivan предложил ставшее революционным и на много лет вперед определившее развитие респираторной медицины сна решение – использовать для лечения СОАС неинвазивную вспомогательную вентиляцию в режиме постоянного положительного давления в дыхательных путях. Сам метод, а вместе с ним и аппарат, получили название СиПАП (СРАР – сокращение от английского continuous positive airway pressure). Суть лечения заключается в том, что нагнетаемый в дыхательные пути под постоянным положительным давлением воздух играет роль пневматического каркаса, предупреждающего вибрацию и смыкание стенок глотки во время сна. Внешне это проявляется исчезновением храпа, а, по сути, приводит к нормализации дыхания во время сна.
Без преувеличения можно сказать, что эта методика уникальна сочетанием высокой эффективности и безопасности. Основным показанием для начала лечения аппаратом СиПАП является тяжелый СОАС. Для таких пациентов это единственная на сегодняшний день адекватная альтернатива трахеостомии, которая после внедрения в клиническую практику СиПАП-терапии практически ушла в историю. Кроме того, данный метод можно рассматривать как вариант лечения у пациентов с апноэ сна средней тяжести или даже в легких случаях при наличии характерных жалоб и исходя из предпочтений пациента.
Следует объяснить больному, что данная терапевтическая методика носит компенсаторный характер, т.е. не ведет к излечению СОАС, но позволяет эффективно его контролировать и поэтому лечение должно проводиться на регулярной основе. Хотя в идеале следует стремиться к тому, чтобы пациент пользовался аппаратом СиПАП каждую ночь и в течение всего времени сна, согласно рекомендациям D. I. Loube et al. (1999) адекватным принято считать сон с прибором в течение как минимум 4-5 часов за ночь не менее 5 дней в неделю.
Аппарат для СиПАП-терапии представляет собой портативный компрессор, работа которого контролируется миникомпьютером. Больной подключается к дыхательному контуру при помощи масок различных модификаций – чаще всего закрывающих только нос, которые закрепляются на лице при помощи специальных эластичных ремней. Для удаления выдыхаемой углекислоты создается постоянная небольшая утечка воздуха из маски через специальный клапан. Маска соединяется с аппаратом при помощи гибкого воздуховодного шланга. Современные аппараты СиПАП портативны, имеют малый вес и отличаются низким уровнем производимого при работе шума.
Принципиально важной является интеллектуальная составляющая большинства современных приборов. Сегодня СиПАП не только осуществляет лечение, но и регистрирует его процесс. Прибор сохраняет в памяти параметры дыхания самого пациента, величину давления и наличие утечек воздуха, остаточные апноэ, гипопноэ и храп. Более того, многие аппараты научились различать обструктивный и центральный характер возникающих респираторных событий. Таким образом, параллельно с лечебной функцией СиПАП как бы играет роль респираторного монитора, контролирующего эффективность собственной работы.
Изначально подбор необходимой величины давления воздуха осуществлялся эмпирически специалистом-медиком, ориентируясь на исчезновения апноэ, гипопноэ и храпа. И это давление в дальнейшем использовалось в качестве фиксированной лечебной величины. Однако, то давления воздуха, которое необходимо пациенту для устранения обструкции верхних дыхательных путей, не является постоянным и зависит от положения тела, глубины сна и других факторов. Это послужило основанием к созданию нового класса лечебных приборов с функцией автоматического подбора лечебной величины давления воздуха в зависимости от потребностей пациента – аппаратов Авто-СиПАП. Обеспечивая лишь то давление, которое реально необходимо больному в каждый конкретный момент времени, такой прибор позволяет сочетать эффективность с максимально возможной комфортностью лечения. При этом в ряде исследований было показано, что при определении необходимой пациенту величины давления с помощью современных аппаратов с автоматической настройкой получаемый результат обычно аналогичен тому, который достигается в ходе подбора лечения на неавтоматическом СиПАП аппарате с участием медицинского персонала. Авто-СиПАП не только существенно упрощает подбор терапии, но и позволяет делать это в амбулаторном режиме. При этом за счет имеющегося программного обеспечения сам прибор одновременно контролирует эффективность проводимого лечения, а нормализация насыщения крови кислородом может отслеживаться с помощью уже обсуждавшейся нами мониторной пульсоксиметрии.
Естественно, как и любой другой медицинский прибор Авто-СиПАП не универсален. Такие аппараты не рекомендуется применять для лечения СОАС у больных с застойной сердечной недостаточностью, тяжелыми обструктивными заболеваниями легких, хронической дыхательной недостаточностью на фоне морбидного ожирения. Тем не менее, существует большое число пациентов с апноэ сна у которых использование автоматического прибора в сочетании с пульсоксиметром потенциально позволяет проводить подбор лечения амбулаторно.
Качество последующей терапии и переносимость лечения во многом зависят от правильного подбора маски. Все маски и воздуховоды имеют стандартные разъемы и поэтому полностью совместимы друг с другом. Это позволяет комплектовать приборы масками не только разных типов и размеров, но и от разных производителей, так как даже незначительные конструктивные отличия в ряде случаев определяют субъективную комфортность для пациента. Задача состоит в том, чтобы подобрать наиболее герметичную при контакте с лицом и при этом удобную для больного маску. Большинство пациентов отдает предпочтение носовым маскам. При этом следует остановиться на наименьшем из возможных размеров, но проконтролировать, чтобы это не провоцировало сдавления носа и ухудшение носового дыхания. Правильность выбора маски и ее фиксации на лице следует проверить, пока больной бодрствует, создав на короткое время нагрузку давлением порядка 10 см водного столба. Если герметичности удается достичь только за счет крайней сильного, сопровождающегося чувством выраженного дискомфорта натяжения крепежных ремней, значит, выбрана неправильная модель маски или ее размер.
Любой современный прибор для СиПАП-терапии может быть оснащен специальной приставкой – подогреваемым увлажнителем. Это позволяет контролировать температуру и влажность вдыхаемого воздуха и предотвращает возникающую у некоторых пациентов в процессе лечения сухость в носоглотке или заложенность носа. Степень нагревания воды подбирается индивидуально и может регулироваться в зависимости от субъективных ощущений больного. Если пациента в процессе лечения беспокоит ощущение сухости, то степень увлажнения недостаточна. Скопление конденсата в маске, напротив, указывает на необходимость уменьшить степень подогрева. На наш взгляд имеет смысл по умолчанию использовать СиПАП в комбинации с увлажнителем. Наш опыт показывает, что даже те пациенты, которые в состоянии пользоваться прибором без функции увлажнения, при использовании увлажнителя обычно отмечают, что процесс лечения стал для них комфортнее.
Подбор СиПАП-терапии начинают с определения того давления воздуха, которое субъективно приемлемо для больного и не будет мешать засыпанию. Наименьший уровень давления воздуха, предусмотренный в большинстве современных аппаратов для СиПАП-терапии, составляет 4 см водного столба, что позволяет эффективно удалять из дыхательного контура выдыхаемую углекислоту. Для большинства пациентов это и станет той величиной воздушного давления, которую они выберут для комфортного засыпания. Однако, в некоторых случаях, чаще – при выраженном ожирении, при малой величине воздушного давления пациенты жалуются на ощущение нехватки воздуха, и адекватное для таких больных стартовое давление может в итоге оказаться порядка 6-8 см водного столба.
Во время сна аппарат будет постепенно повышать давление воздуха, добиваясь устранения обструкции верхних дыхательных путей. В результате эффективное лечебное давление в некоторые моменты может превысить стартовое в несколько раз. В большинстве случаев это не является проблемой, так как субъективное восприятие давления воздуха во сне и в бодрствовании различаются. Однако отдельным пациентам с тяжелой формой СОАС требуется столь большая величина лечебного давления, что это значительно затрудняет выдох и нарушает сон. Решением такой проблемы может стать предусмотренная во многих моделях СиПАП функция снижения давления во время выдоха. При амбулаторном подборе СиПАП-терапи мы советуем по умолчанию активировать эту опцию.
Иногда после начала лечения вместо исчезнувших обструктивных возникают центральные апноэ и гипопноэ – так называемое комплексное апноэ сна. Предполагают, что это может быть связано с процессами торможения в дыхательном центре, который длительное время был адаптирован к условиям гипоксемии и гиперкапнии и не успевает перестроиться вслед нормализовавшемуся газообмену. Современный высокотехнологичный СиПАП в этом случае сам определит, что наблюдаемые дыхательные аномалии носят именно центральный характер. В ряде случаев такие центральные нарушения дыхания проходят самостоятельно спустя несколько ночей лечения. Если же это не происходит, то такому пациенту показан другой, более сложный чем СиПАП лечебный алгоритм, и его следует направить для подбора терапии в специализированный сомнологический центр.
Традиционная схема инициации СиПАП-терапии предполагает определение необходимых лечебных параметров в течение одной ночи. И если результаты первичного подбора лечения удовлетворительны, а пациент в дальнейшем планирует использование автоматической модели СиПАП, то теоретически на этом можно остановиться.
Если же больной настроен на лечение аппаратом с фиксированной величиной давления, то результатов первой ночи может оказаться недостаточно. Дело в том, что после устранения СОАС у пациента возникает рикошет сна – если до начала лечения сон был ненормально поверхностным, то тут он становится аномально глубоким, что требует более высокого давления для коррекции апноэ. Кроме того, постоянное спадение стенок глотки во время сна ведет к хронической травме и отеку, что в свою очередь усугубляет нарушения дыхания. Через несколько ночей на фоне проводимого лечения нормализуется структура сна, уходит отек слизистой оболочки верхних дыхательных путей и необходимое для коррекции СОАС давление может стать несколько меньше.
Степень наблюдающегося у пациента субъективного улучшения самочувствия обычно прямо пропорциональна исходной выраженности симптомов болезни. Естественно, что чем больший эффект от терапии бывает получен, тем более мотивированным в отношении дальнейшее лечение оказывается больной. Соответственно пациенты с тяжелым СОАС в дальнейшем чаще продолжают регулярно использовать аппарат СиПАП в амбулаторных условиях, а самым надежным контролером для них становится само заболевание, симптомы которого достаточно быстро возвращаются при несоблюдении правильного режима лечения. Если же симптоматика изначально выражена умеренно или слабо, то бывает затруднительно убедить больного в необходимости лечения на постоянной основе, так как в этом случае испытываемый ночью дискомфорт может субъективно перевесить потенциальную пользу.
К сожалению, немалое число пациентов в итоге не соблюдает адекватный режим лечения, либо вообще отказывается от него. Это может быть вызвано нежеланием лечиться постоянно, физическим или психологическим дискомфортом при использовании лечебного оборудования, относительной дороговизной аппаратов СиПАП. По нашим наблюдениям, лучшую комплаентность потенциально можно ожидать от работающих мужчин старше 50 лет, с высшим образованием, уровнем доходов не ниже среднего и страдающих тяжелым СОАС. Однако, во многих случаях предсказать долгосрочную приверженность того или иного пациента к лечению на практике бывает затруднительно. Пробный курс СиПАП-терапии в домашних условиях длительностью порядка 5-7 ночей позволяет пациенту лучше определиться со своим отношением к этой процедуре, а врачу точнее прогнозировать дальнейшие перспективы лечения. Кроме того, за это время можно окончательно скорректировать лечебный режим и определиться с моделью прибора, а также типом и размером маски, которыми пациент в перспективе станет пользоваться, привить ему навыки пользования лечебной аппаратурой. Показано, что правильное обучение пациента во многом определяет дальнейшее соблюдение им адекватного режима лечения.
В связи с отсутствием в нашей стране соответствующей патронажной службы по оказанию больным с СОАС консультативной помощи и контролю проведения СиПАП-терапии на дому, эти функции автоматически возлагаются на лечащего врача. Меньшая стоимость амбулаторного лечения пациента по сравнению со стационаром и, особенно, специализированным медицинским центром, делает такое более длительное пребывание под врачебным наблюдением допустимым и оправданным. Конечно, собственных ресурсов лечебного учреждения может оказаться недостаточно, чтобы обеспечить каждого больного с СОАС аппаратурой для подобной тестовой терапии, но проблема легко решаема, так как многие продавцы лечебного оборудования предоставляют своим потенциальным покупателям услугу предпродажной аренды аппаратов СиПАП.
Одной из нередко встречающихся при начале СиПАП-терапии проблем, про возможность которой следует помнить, так как это может стать причиной недостаточной эффективности и плохой переносимости лечения, является утечка воздуха. В результате прибор оказывается не в состоянии поддерживать необходимое давление в дыхательных путях, и алгоритм лечения оказывается нарушен. При амбулаторном подборе СиПАП-терапии определенная сложность связана с тем, что врач не имеет возможности отследить наличие значимой утечки в режиме реального времени. Однако так как современные аппараты в числе прочего умеют регистрировать и сохранять в памяти данные о наличии и объеме утечек воздуха, это существенно облегчает анализ и интерпретацию проблемной ситуации.
Существует два вида утечек – из маски и через рот. Утечка из-под маски обычно происходит в результате неправильно подобранного размера или недостаточно плотной ее фиксации на лице, что легко устранимо. Другим вариантом утечки при использовании для лечения наиболее распространенных носовых масок является стравливание воздуха через рот. Часто это оказывается связано с высоким уровнем лечебного давления или существенным затруднением носового дыхания. При значительных утечках воздуха через рот можно предложить больному попробовать заменить носовую маску на ротоносовую модель.
Если длительность лечения в течение ночи адекватна, значимые утечки отсутствуют, дыхательные нарушения во время сна устранены и переносимость СиПАП-терапии хорошая, но пациента к концу пробного курса лечения продолжает беспокоить сонливость, имеет смысл направить его в специализированный сомнологический центр для выявления других возможных заболеваний, способных вызывать аналогичную симптоматику.
В заключении разговора об амбулаторной диагностике и лечении СОАС хотелось бы поделиться интересным на наш взгляд историческим наблюдением. Вплоть до начала 90-х годов прошлого века использование диагностических приборов на базе пульсоксиметрии рассматривалось нашими зарубежными коллегами в качестве одной из правомочных диагностических тактик при подозрении на наличие СОАС. Предложенная C. E. Sullivan методика лечения апноэ сна с помощью аппарата СиПАП первоначально была встречена частью врачей довольно скептически и только спустя несколько лет стала восприниматься как метод выбора при лечении СОАС. Но затем в 1993 году на рассмотрение Конгресса и министерства здравоохранения США был представлен доклад Национальной комиссии по исследованию расстройств сна с говорящим самим за себя названием «Проснись, Америка: предупреждение нации о проблемах сна». В числе прочего в документе большое внимание уделялось обструктивному апноэ сна и его последствиям как для пациентов, так и для общества в целом. В результате в Соединенных Штатах был организован Национальный центр по исследованию расстройств сна и принята Национальная программа по борьбе с нарушениями сна. Это дало мощный толчок развитию медицины сна как в Северной Америке, так и в Западной Европе. И вскоре многие эксперты начали высказываться в том ключе, что одна только пульсоксиметрия не должна использоваться для диагностики СОАС, в то время как кардиореспираторное мониторирование является достаточным с медицинской и оптимальным с экономической точки зрения. А уже на рубеже 2000-х годов стала активно продвигаться концепция, согласно которой кардиореспираторное мониторирование должно занять нишу первичного скрининга, а стандартом диагностики следует считать полисомнографию. Эти принципиальные изменения диагностических и лечебных стратегий наглядно иллюстрируют как этапы эволюции, которые проделала медицина сна в этих странах, так и состояние финансирования этой области здравоохранения.
Хочется думать, что российская сомнология также находится на пороге подъема, и в ближайшем будущем полисомнография станет для отечественных врачей рутинной диагностической процедурой, а назначение СиПАП-терапии столь же обычным, как лечение с помощью лекарственных средств. Но это в перспективе, а страдающие СОАС пациенты нуждаются во врачебной помощи сейчас. Применительно к проблеме обструктивного апноэ сна многие компоненты полисомнографии далеко не всегда обязательны для повседневной клинической практики. Главными атрибутами диагностики СОАС являются оценка носового или ротоносового потока воздуха, пульсоксиметрия и дыхательная экскурсия грудной клетки и живота. Причем в отдельных, наиболее ярких случаях одной только пульсоксиметрии, пусть и с оговорками, бывает достаточно. СОАС узнаваем клинически, может быть оценен количественно, его диагностика и принципы лечения отработаны и поддаются алгоритмизации.
Чтобы успешно помочь пациенту с обструктивным апноэ сна, врач для начала должен просто хорошо знать эту проблему. И тогда, как показывает наш опыт, даже при наличии минимального необходимого набора медицинской аппаратуры можно, в том числе и амбулаторно, выявлять и лечить значительную часть больных с СОАС в лечебных учреждениях терапевтического профиля. Мы признаем, что на практике это получается не всегда, но кто хочет добиться результата – ищет средства, а кто не хочет – причины.
ЛИТЕРАТУРА:
- Cao M. T., Guilleminault C., Kushida C. A. Clinical Features and Evaluationof Obstructive Sleep Apnea and Upper Airway Resistance Syndrome // Principles and practice of sleep medicine. – 5-th Ed. – Missouri: Elsevier Inc., 2011. – Р.1206-1218.
- Burwell C. S., Robin E. D., Whaley R. D., Bickelmann A. G. Extreme obesity associated with alveolar hypoventilation – a Pickwickian syndrome // Am. J. Med. – 1956. – Vol. 21. –
P. 811 - 818. - Guilleminault C., Eldridge F.L., Dement W.C. Insomnia with sleep apnea: a new syndrome // Science. – 1973. – Vol.181. – P.856-858.
- Chobanian A.V., Bakris G.L., Black H.R. et al. National Heart, Lung, and Blood Institute, Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure; National High Blood Pressure Education Program Coordinating Committee. The Seventh Report of the Joint NationalCommittee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure: the JNC 7 report // JAMA. – 2003. – Vol.289 – P.2560 -2572.
- Marin J.M., Carrizo S.J., Vicente E., Agusti A.G. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study // Lancet. – 2005. – Vol.365. – P.1046-1053.
- Fletcher E. C. The relationship between systemic hypertension and obstructive sleep apnea: facts and theory // Am. J. Med. – 1995. – Vol.98. – P. 118-128.
- Garrigue S., Pepin J.L., Defaye P. et al. High prevalence of sleep apnea syndrome in patients with long-term pacing: the European Multicenter Polysomnographic Study // Circulation. – 2007. – Vol.115. – P.1703-1709.
- Young T., Finn L., Peppard P.E. et al. Sleep disordered breathing and mortality: eighteen-year follow-up of the Wisconsin sleep cohort // Sleep. – 2008. – Vol.31. – P.1071-1078.
- Hla K.M., Young T., Hagen E.W. et al. Coronary heart disease incidence in sleep disordered breathing: the Wisconsin Sleep Cohort Study // Sleep. – 2015. – Vol.38. – Р.677-684.
- Зильбер А. П. Синдромы сонного апноэ. – Петрозаводск: Изд-во Петрозаводск. ун-та, 1994.
- Tregear S., Reston J., Schoelles K., Phillips B. Obstructive sleep apnea and risk of motor vehicle crash: systematic review and meta-analysis // J. Clin. Sleep Med. – 2009. – Vol.5. – P.573-581.
- Krieger J. Clinical presentation of sleep apnea // European respiratory monograph. – 1998. – Vol. 3, Monograph 10. – P. 75-105.
- Бузунов Р.В., Легейда И.В., Царева Е.В. Храп и синдром обструктивного апноэ сна у взрослых и детей: Практическое руководство для врачей. – М., 2013.
- Lugaresi E., Plazzi G. Heavy snorer disease: from snoring to the sleep apnea syndrome – an overview // Respiration. 1997. – Vol.64, Suppl. 1. – P.11-14.
- Flemons W.W. Obstructive sleep apnea // N. Engl. J. Med. – 2002. – Vol.347. – P.498-504.
- Hoffstein V., Szalai J.P. Predictive value of clinical features in diagnosing obstructive sleep apnea // Sleep. – 1993. – Vol.16. – P.118-122.
- Douglas N.J. ABC of sleep disorders. The sleep apnoea-hypopnoea syndrome and snoring // BMJ. – 1993. – Vol.306. – P.1057-1060.
- Воронин И.М. Кардиоваскулярные последствия обструктивных нарушений дыхания во время сна. – Тамбов: Изд-во ТГУ им. Г.Р. Державина, 2001.
- Диагностика и лечение артериальной гипертензии: Российские рекомендации (четвертый пересмотр). – Всероссийское научное общество кардиологов. – М., 2010.
- Walia H.K., Li H., Rueschman M. et al. Association of severe obstructive sleep apnea and elevated blood pressure despite antihypertensive medication use // J. Clin. Sleep Med. – 2014. – Vol.10. – P.835-843.
- Sleep-Related Breathing Disorders in Adults: Recommendations for Syndrome Definition and Measurement Techniques in Clinical Research. The Report of an American Academy of Sleep Medicine Task Force // Sleep. – 1999. – Vol. 22. – P.667-689.
- Chesson A. L., Berry R. B., Pack A. Practice Parameters for the Use of Portable Monitoring Devices in the Investigation of Suspected Obstructive Sleep Apnea in Adults // Sleep. – 2003. – Vol. 26. – P. 907-913.
- Somers V. K., White D. P., Amin R. et al. Sleep Apnea and Cardiovascular Disease //
J. Amer. Coll. Card. – 2008. Vol. 52. Р.686-718. - Collop N. A., Anderson W. M., Boehlecke B. et al. Clinical Guidelines for the Use of Unattended Portable Monitors in the Diagnosis of Obstructive Sleep Apnea in Adult Patients // J. Clin. Sleep Med. – 2007. – Vol. 3. – P.737-747.
- Epstein L. J., Kristo D., Strollo P. J. et al. Clinical Guideline for the Evaluation, Management and Long-term Care of Obstructive Sleep Apnea in Adults // J. Clin. Sleep Med. – 2009. – Vol.5. – P.263-276.
- Fleetham J., Ayas N., Bradley D. Canadian Thoracic Society 2011 guideline update: Diagnosis and treatment of sleep disordered breathing // Can. Respir. J. – 2011. – Vol 18. – Р.25-47.
- Guilleminault C., Connolly S. J., Winkle R. A. Cardiac arrhythmia and conduction disturbances during sleep in 400 patients with sleep apnea syndrome // Am. J. Cardiol. – 1983. – Vol.52. – P.490-494.
- Mehra R., Benjamin E.J., Shahar E. et al. Association of nocturnal arrhythmias with sleep-disordered breathing: The Sleep Heart Health Study // Am. J. Respir. Crit. Care Med. – 2006. – Vol.173. – P.910 –916.
- Zwillich C., Devlin T., White D. et al. Bradycardia during sleep apnea. Characteristics and mechanism // J. Clin. Invest. – 1982. – Vol.69. – P.1286-1292.
- Yamashiro Y., Kryger M.H. Nocturnal oximetry: is it a screening tool for sleep disorders? // Sleep. 1995. – Vol.18. – P.167-171.
- Gyulay S., Olson L.G., Hensley M. J. et al. A comparison of clinical assessment and home oximetry in the diagnosis of obstructive sleep apnea // Am. Rev. Respir. Dis. – 1993. –
Vol. 147. – P.50-53. - Levy P., Pepin J. L., Deschaux-Blanc C. et al. Accuracy of oximetry for detection of respiratory disturbances in sleep apnea syndrome // Chest. – 1996. – Vol. 109. –
P. 395–399. - Ryan P.J., Hilton M.F., Boldy D.A. et al. Validation of British Thoracic Society guidelines for the diagnosis of the sleep apnoea/hypopnoea syndrome: can polysomnography be avoided? // Thorax. – 1995. – Vol.50. – P.972-975.
- Williams A. J., Yu G., Santiago S., Stein M. Screening for sleep apnea using pulse oximetry and a clinical score // Chest. – 1991. – Vol. 100. – P. 631–635.
- Farre R., Montserrat J.M., Ballester E. et al. Importance of the pulse oximeter averaging time when measuring oxygen desaturation in sleep apnea // Sleep. – 1998. – Vol. 21. – P.386-390.
- Mechanick J.I., Kushner R.F., Sugerman H.J. et al. American Association of Clinical Endocrinologists, The Obesity Society and American Society for Metabolic & Bariatric Surgery Medical guidelines for clinical practice for the perioperative nutritional, metabolic, and nonsurgical support of the bariatric surgery patient // Endocr. Pract. – 2008. – Vol.14, Suppl.1. – P.1-83.
- Chesson A.L., Berry R.B., Pack A. et al. Practice parameters for the use of portable monitoring devices in the investigation of suspected obstructive sleep apnea in adults // Sleep. – 2003. – Vol.26. – P.907-913.
- Kushida C.A., Morgenthaler T.I., Littner M.R. et al. Practice parameters for the treatment of snoring and obstructive sleep apnea with oral appliances: an update for 2005 // Sleep. – 2006. – Vol.29. – P. 240-243.
- Kushida C.A., Littner M.R., Hirshkowitz M. et al. Practice parameters for the use of continuous and bilevel positive airway pressure devices to treat adult patients with sleep-related breathing disorders // Sleep. – 2006. – Vol. 29. – P.375-380.
- Littner M., Kushida C.A., Hartse K. et al. Practice parameters for the use of laser-assisted uvulopalatoplasty: an update for 2000 // Sleep. – 2001. – Vol.24. – P.603-619.
- Littner M., Hirshkowitz M., Davila D. et al. Practice parameters for the use of auto-titrating continuous positive airway pressure devices for titrating pressures and treating adult patients with obstructive sleep apnea syndrome // Sleep. – 2002. – Vol.25. – P.143-147.
- Morgenthaler T.I., Kapen S., Lee-Chiong T. et al. Practice parameters for the medical therapy of obstructive sleep apnea // Sleep. – 2006. – Vol.29. – P.1031-1035.
- Kuhlo W., Doll E., Franck M.C. Erfolgreiche Behandlung eines Pickwick-Syndroms durch eine Dauertrachealkanüle // Dtsch. Med. Wochenschr. – 1969. – Vol.94. – P.1286-1290.
- Lugaresi E., Coccagna G., Mantovani M., Brignani F. Effects of tracheotomy in hypersomnia with periodic respiration // Rev. Neurol. – 1970. – Vol.123. – P.267-268.
- Wake up America: a national sleep alert. A report of the National Commission on Sleep Disorders Research. – Washington, 1993.
- Loube D.I., Gay P.C., Strohe K.P. et al. Indications for positive airway pressure treatment of adult obstructive sleep apnea: a consensus statement // Chest. – 1999. – Vol.115. –
P.863-866. - Parati G., Lombardi C., Hedner J. et al. Position paper on the management of patients with obstructive sleep apnea and hypertension: joint recommendations by the European Society of Hypertension, by the European Respiratory Society and by the members of European COST (COoperation in Scientific and Technological research) ACTION B26 on obstructive sleep apnea // J. Hypertens. – 2012. – Vol.30. – P.633-646.
